单细胞RNA分析表明第三代CAR-T细胞的内在功能特征与淋巴瘤疗效相关
本期文献[1]导读
-
对CAR-T细胞产品进行单细胞分析可发现与疗效相关的T细胞亚群。
-
在制备CAR-T细胞的过程中保持较短的体外扩增时间会产生更多具有功能性的CAR-T细胞。
-
具有高多功能指数、高细胞毒性和细胞因子分泌特征/表型以及低功能障碍表型的CD8+ CAR-Ts与CAR-T细胞治疗淋巴瘤的缓解相关
研究背景
靶向CD19的嵌合抗原受体T(CAR-T)细胞疗法用于B细胞恶性肿瘤具有显著疗效,但大部分患者未实现长期临床缓解。既往研究表明,与CAR-T细胞治疗缓解相关的参数(包括疾病组织学和清淋预处理方案、疾病类型、CAR-T输注产品的特性以及CAR-T细胞制备材料(采集的患者T细胞)的状态)均会影响大B细胞淋巴瘤(LBCL)患者对CD19 CAR-T治疗的缓解。
研究方法
本项II期、开放标签、单臂、单中心研究,纳入在瑞典乌普萨拉大学医院接受1剂或2剂第三代CD19 CAR-T细胞治疗的弥漫性大B细胞淋巴瘤(DLBCL)或白血病患者,使用单细胞RNA测序和多色流式细胞术对CAR-T输注产品进行了详细表征描述,以确定具有细胞因子和细胞毒性等特征的效应CD8+ CAR-T细胞亚群与临床缓解的相关性。
研究结果
患者特征、CAR-T治疗方案、临床缓解情况和安全性特征
共纳入28例患者,其中24例患者接受了CAR-T治疗(图1A)。患者疾病类型包括:DLBCL(n=21)、惰性B细胞淋巴瘤(n=2)(滤泡性淋巴瘤,n=1;边缘区淋巴瘤,n=1)和急性淋巴细胞白血病(ALL)(n=1)(图1B)。CAR-T治疗前的患者特征如图1B所示。患者接受1剂 (n=10) 或2剂CAR-T (n=14)治疗(图 1A),仅在第1剂时进行预处理。10例患者由于CAR-T相关不良事件未接受第2剂CAR-T治疗。4 例患者因CAR-T制备失败 (n=1) 或疾病快速进展 (n=3) 未接受CAR-T治疗。
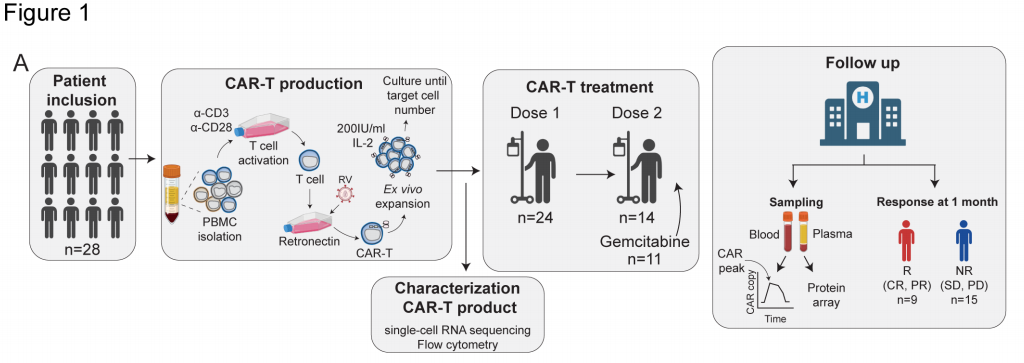
图1A 临床研究中从患者入组、CAR-T制备和治疗到随访的示意图
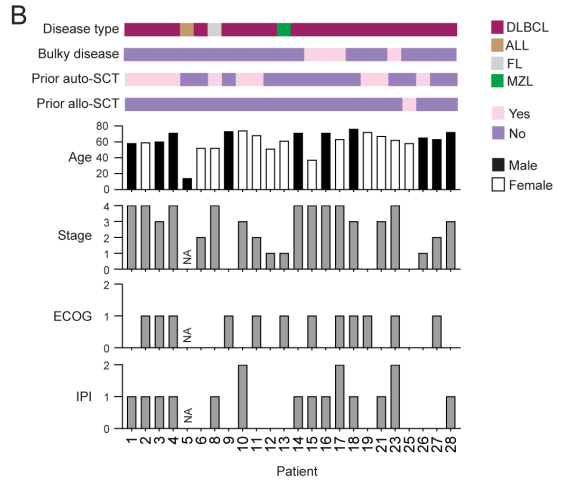
图1B CAR-T输注前的患者特征
首剂CAR-T输注后,1个月的总缓解率(ORR)率[完全缓解(CR)+部分缓解(PR)]为38%(9/24),最佳ORR为50%(12/24)(图1C)。
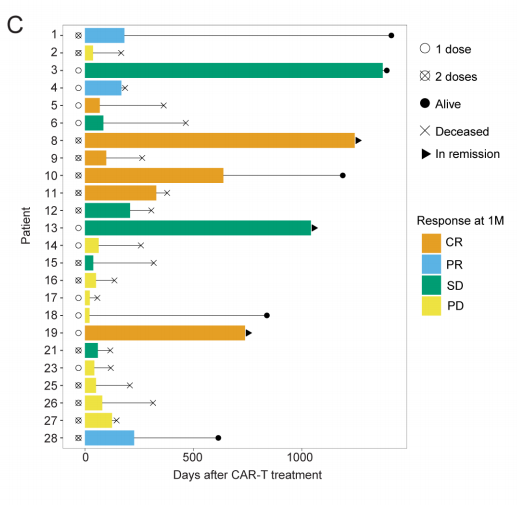
图1C 患者结局和CAR-T输注次数的泳道图
将患者分为缓解者和未缓解者两类。如果患者在1个月的随访中达到影像学缓解,则定义为缓解者(R,n=9);如果未达到影像学缓解,则定义为未缓解者(NR,n=15)。
仅有4例患者发生3级CRS,无患者发生3级免疫效应细胞相关神经毒性综合征 (ICANS)。7例患者在CAR-T治疗后发生严重血细胞减少症。
CAR-T产品的单细胞RNA测序和聚类分析
通过单细胞RNA测序 (scRNA-seq) 研究CAR-T输注产品质量对患者结局的影响。分析样本来自23例接受治疗的淋巴瘤患者(排除ALL患者)的CAR-T细胞(图2A)。通过无监督聚类识别出12个簇(0-11)(图2D),几乎所有患者中均存在每个簇的细胞(图2E)。
使用scRNA-seq测定CD8与CD4的表达(图2F,2G)。在所有簇中均检测到CAR-T输注产品中CAR转导的T细胞(图2H)。大多数 CAR-T输注产品均存在CD8+ CAR-T细胞。
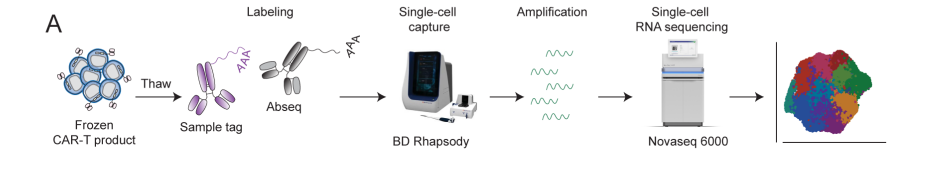
图2A 制备用于单细胞RNA测序的患者衍生CAR-T产品的实验程序示意图
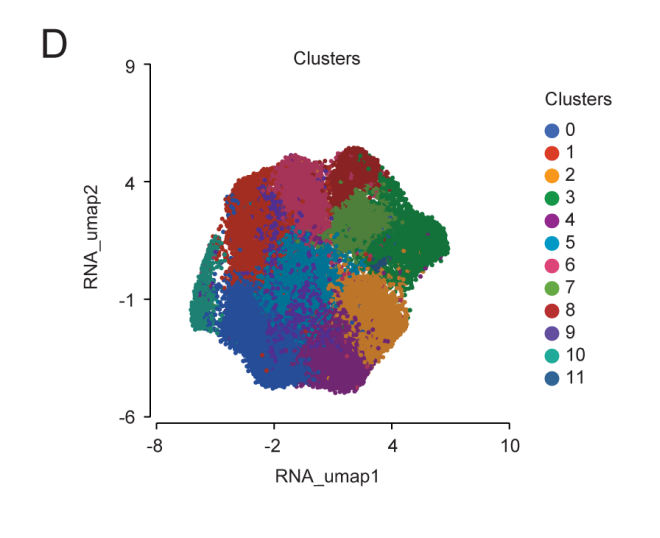
图2D UMAP显示12个已识别T细胞簇 (0-11) 的定位
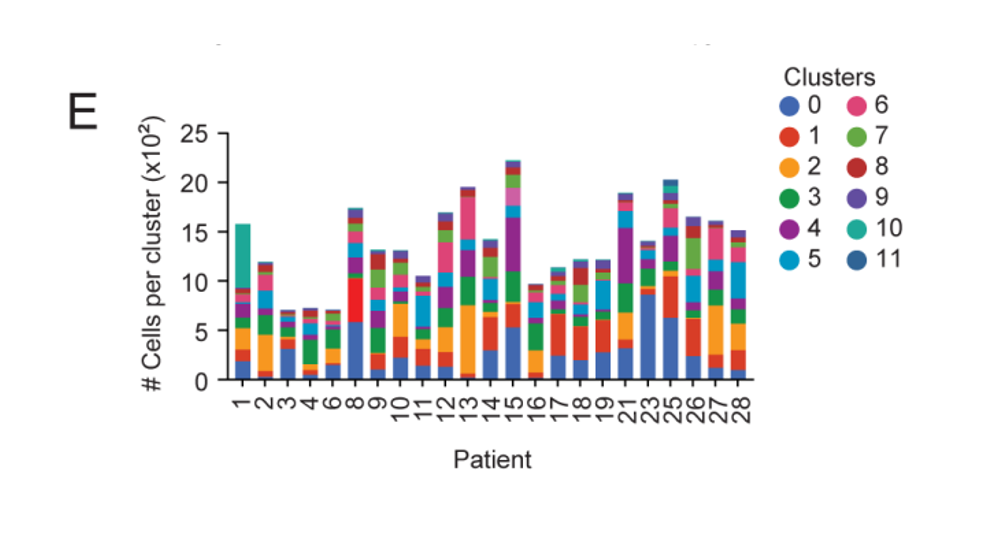
图2E 条形显示每例患者每个簇中的细胞总数
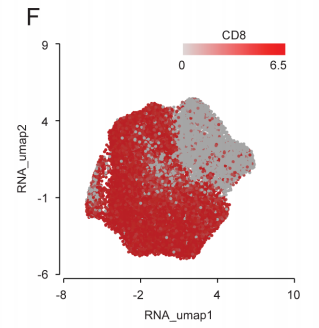
图2F UMAP显示的CD8+ CAR-T细胞
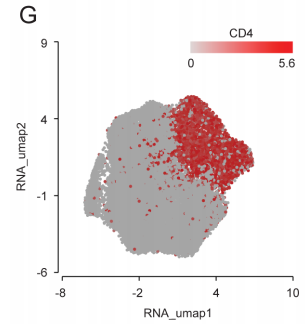
图2G UMAP显示的CD4+T细胞
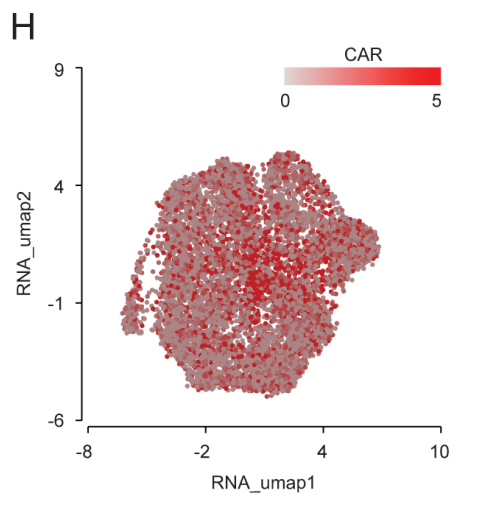
图2H UMAP显示的CAR+T细胞
CAR-T产品中效应CD8+ CAR-T细胞具有高细胞毒性和细胞因子特征/表型
缓解者和未缓解者的CD8+ CAR-T细胞比较结果显示,疾病缓解与细胞毒性(例如穿孔素1[PRF1]、颗粒酶2[GZMB]、人颗粒溶素[GNLY])和细胞因子产生(例如趋化因子配体3[ CCL3]、趋化因子配体4[CCL4]、干扰素-γ[IFN-γ])等效应功能相关的基因上调相关(图3B)。
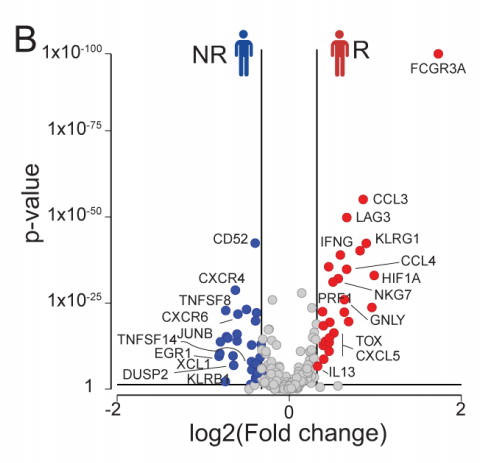
图3B 缓解者(R)和未缓解者(NR)中差异表达基因的火山图
通过无监督聚类分析识别的12个簇中,9个簇带有CD8+ CAR-T细胞(图3D)。虽然每个识别的簇中都存在缓解者和未缓解者的细胞,但每个簇中各组细胞的分布各不相同(图3E、3F)。对每个簇中的差异基因表达和既往描述的基因特征(细胞毒性、细胞因子、细胞周期、细胞耗竭和功能障碍)进行AUCell分析,确定输注产品中存在的T细胞亚群和细胞内在功能(图3D)。缓解者具有与细胞毒性和细胞因子分泌相关基因上调的特征(图3G)。未缓解者的CD8+ CAR-Ts细胞具有功能失调的基因特征(图3G)。
总之,具有相对较高比例的效应CD8+ CAR-Ts细胞(具有表达细胞毒性和细胞因子分泌因子的效应T细胞表型)的CAR-T输注产品与更好的临床缓解相关。
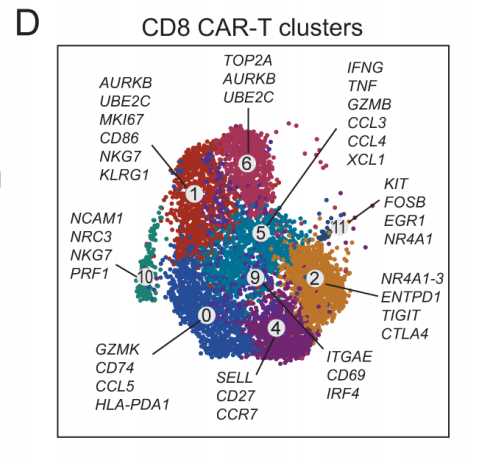
图3D UMAP显示由无监督聚类生成的CD8+ CAR-T细胞簇
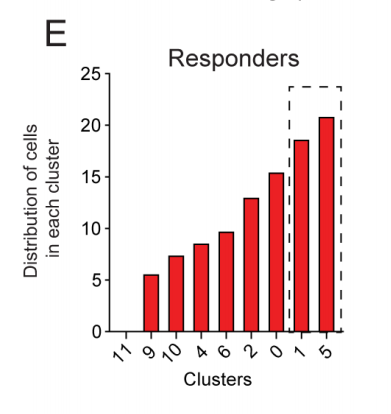
图3E 缓解者每个CD8+ CAR-T细胞簇内的细胞分布
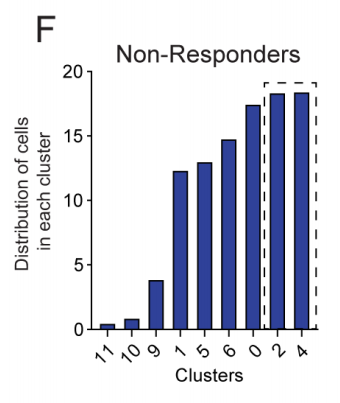
图3F 未缓解者每个CD8+ CAR-T细胞簇内的细胞分布

图3G 缓解者和未缓解者功能状态的AUCell评分
缓解相关的CD8+ CAR-T细胞亚群比例增加与CAR-T制备过程中较短的体外扩增时间有关
与未缓解者的CAR-T产品相比,缓解者的CAR-T输注产品在体外制备过程中扩增性能更好,体外培养时间更短。为确定体外培养时间对CAR-T产品的影响,本文研究了基因表达和体外培养时间的相关性(图3H)。结果显示93个基因(如淋巴细胞激活分子家族成员7[SLAMF7],CD69,T细胞免疫球蛋白和ITIM结构域蛋白[TIGIT],双特异性磷酸酶1[DUSP1])与培养时间呈正相关,129个基因(如CCL3,CCL4,GZMB,GLNY,IFN-γ,NKG7,PRF1,KLRGI,MK167)与培养时间呈负相关。与培养时间延长(表达减少)呈负相关的129个基因中,有64个基因在缓解者中上调(图3I)。一些常见的基因与细胞毒性和细胞因子分泌有关,并且在CAR-T制备过程培养时间较长的产品中,缓解者富集效应样CD8+ CAR-T细胞的比例较低(簇5)(图3I,3J)。
总之,CAR-T生产过程中的体外培养时间会对细胞毒性和细胞因子分泌特征的表达产生不利影响。体外培养时间较短的CAR-T产品可富集更多与缓解相关的效应CD8+ CAR-T细胞亚群。
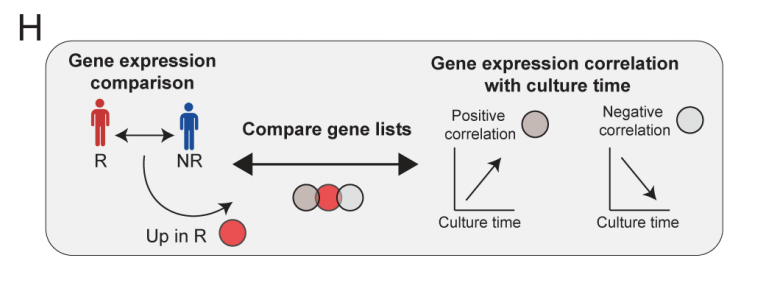
图3H 缓解者 (R) 中随培养时间变化的基因表达(上调或下调)示意图
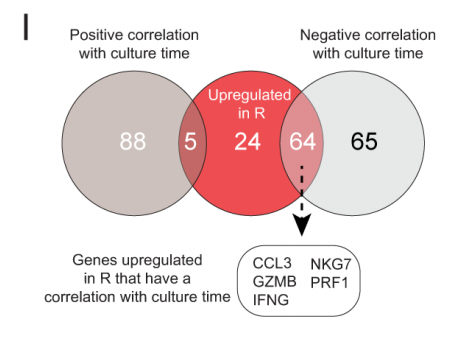
图3I 将与培养时间呈负相关(下调)和正相关(上调)的基因与缓解者(R)的CD8+ CAR-T细胞中特异性上调的基因进行比较
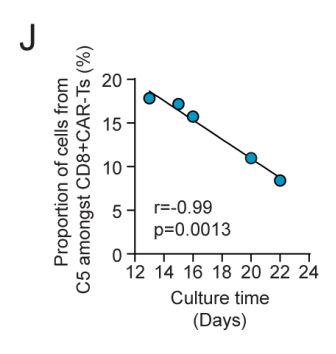
图3J 制备过程中不同时间点收获的CAR-T产品中来自簇5的CD8+ CAR-T细胞的比例
CAR-T细胞产品高多功能异质性与临床缓解相关
鉴于缓解者输注的CAR-T产品具有更多的效应T细胞,研究评估了CAR-T产品的多功能性。CAR-T细胞的单细胞多功能强度指数(scPSI)定义为每个细胞共表达来自预先指定的分类列表中2个或多个标记物的CAR-T细胞,与相应基因的表达水平相关(图4A)。输注产品中的大多数CD8+ CAR-T细胞共表达2个或3个基因,而少数细胞共表达4个或更多基因(图4B)。CAR-T产品具有广泛的scPSI值,大多数CAR-T细胞具有化学吸引表达谱,其次是效应表达谱(图4C)。与未缓解者相比,缓解者的CAR-T输注产品中多功能CAR-T细胞的总分数(图4D)和全球平均scPSI更高(图4E)。多功能细胞的分数(图4F)和scPSI(图4G)不随CAR-T体外扩增时间延长而改变。无论体外培养时间如何,缓解者的CAR-T细胞的scPSI总是高于未缓解者。结果表明,CAR-T产品中高多功能CD8+ CAR-T细胞的比例和及其细胞因子表达水平与临床缓解相关。
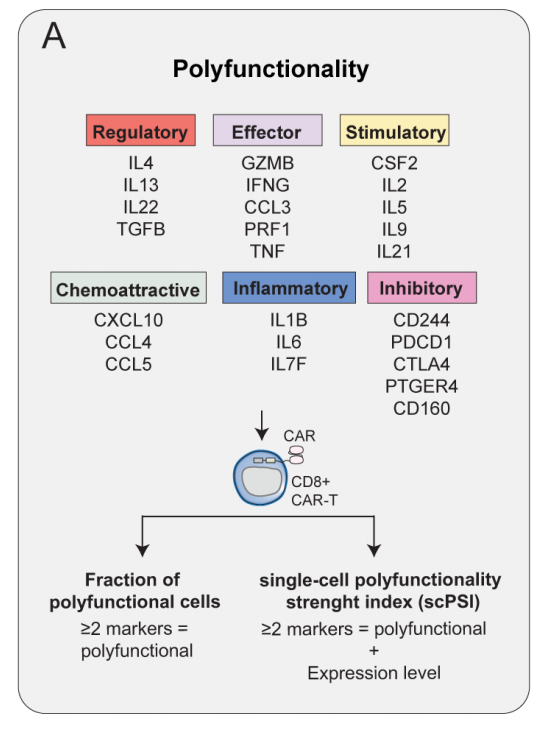
图4A CAR-T的多功能性通过单细胞多功能性强度指数 (scPSI) 进行衡量
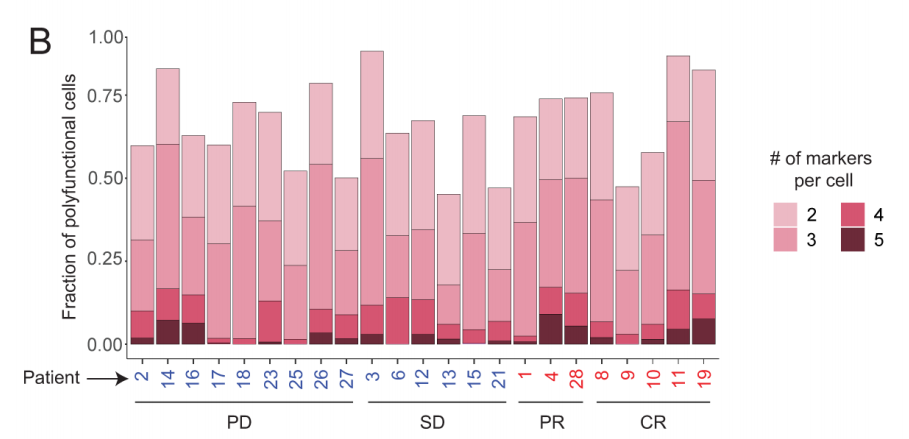
图4B 所有患者中含2个或多个基因(图A中指定)的CD8+ CAR-T细胞比例
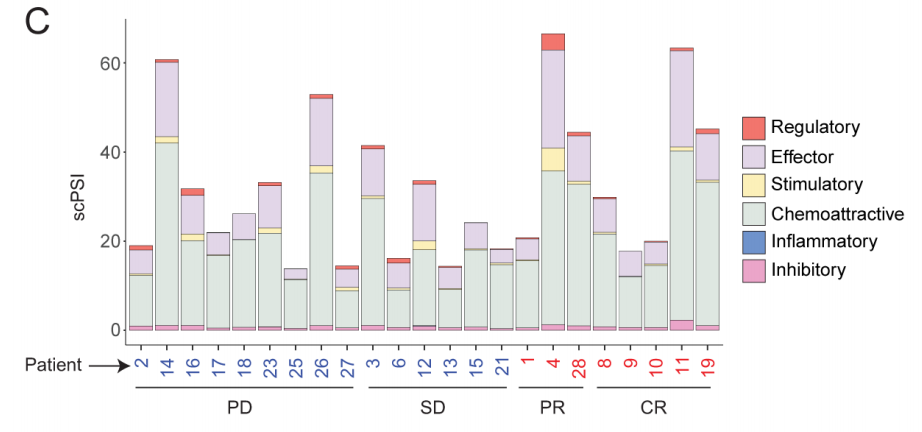
图4C 基于多功能分类,所有患者CD8+ CAR-T细胞的scPSI
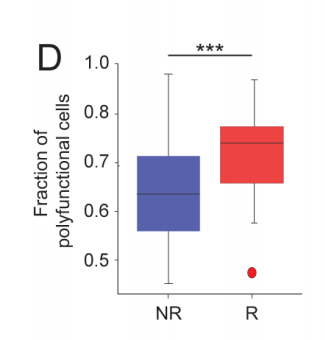
图4D 缓解者 (R) 和未缓解者 (NR) 含2个或多个功能基因的CD8+ CAR-T细胞分数
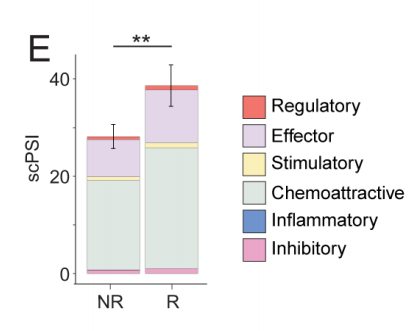
图4E 基于多功能分类,缓解者 (R) 和未缓解者(NR)CD8+ CAR-T细胞的scPSI

图4F 缓解者 (R) 和未缓解者(NR)2个或多个基因的CD8+ CAR-T细胞分数与培养时间的关系
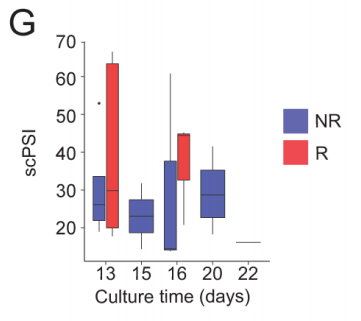
图4G 缓解者 (R) 和未缓解者(NR)的CD8+ CAR-T细胞的scPSI与培养时间的关系
缓解者的CAR-T细胞输注产品具有更多的低功能障碍表型的CD8+ CAR-T细胞
通过流式细胞术在蛋白质水平比较缓解者和未缓解者CAR-T产品中的细胞功能状态(图5A)。未缓解者输注产品中的CAR-T细胞增加了早期T细胞功能障碍标记物CD40L(图5B)和免疫检查点受体重组人T细胞膜蛋白3(TIM-3)蛋白表达增加(图5C)。此外,缓解者CD8+ CAR-Ts细胞中CD45RA+CCR7-效应CAR-Ts细胞(TE)的比例较高(图5D,5E),而缓解较差患者CD45RA-CCR7-效应记忆CAR-Ts细胞(TEM)的比例较高(图5E)。CD45RA-CCR7+中央记忆型CAR-T细胞(TCM)的频率无差异,但缓解者中初始T细胞 (TN) 的比例有增加的趋势(图5E)。此外,缓解者未刺激的CD45RA+CCR7- TE CAR-T细胞表达更高水平的趋化因子(CCL4、CCL3)和细胞毒性分子(GZMB、PRF1)(图5)。在未刺激的TE CAR-T细胞中未观察到IFN-γ或TNF-α表达。以上数据支持效应CD8+ CAR-T细胞对于单细胞RNA测序数据中临床缓解的重要性。
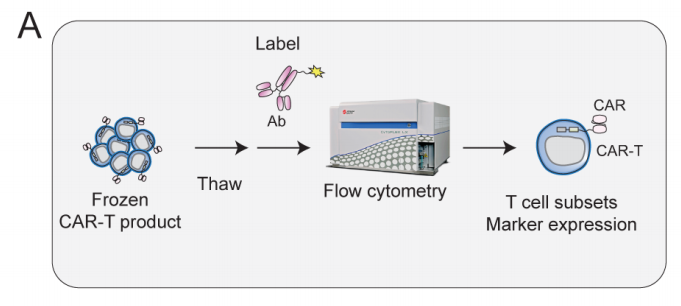
图5A 通过流式细胞术在蛋白质水平上对CAR-T输注产品进行体外表征的示意图
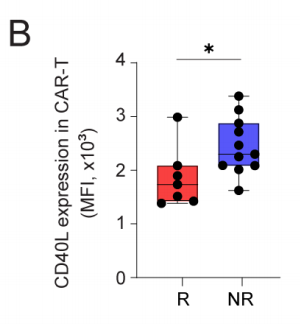
图5B 缓解者(R;n=7)和未缓解者(NR,n=11)的CAR-T细胞上CD40L表达的平均荧光强度 (MFI)
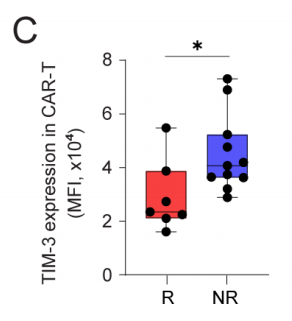
图5C 缓解者(R;n=7)和未缓解者(NR,n=11)的CAR-T细胞上TIM-3表达的平均荧光强度 (MFI)

图5D 具有代表性的效应T细胞(TE, CD45RA+CCR7-)、初始T细胞(TN,CD45RA+CCR7+)、中央记忆型T细胞(TCM,CD45RA-CCR7+)、效应记忆T细胞(TEM,CD45RA-CCR7-)CD8+ CAR-Ts门控策略

图5E 缓解者(R;n=8)和未缓解者(NR;n=14)的CD8+ CAR-T细胞中TE、TN、TCM和TEM的百分比
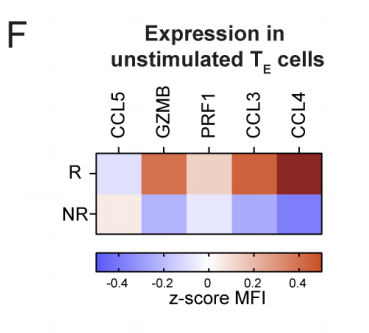
图5F 抗原刺激前,缓解者(R;n=8)和未缓解者(NR;n=14)的CD8+ CAR-T细胞上标记物表达的平均Z评分
此外,缓解者中表达细胞毒性分子(IFN-γ,TNF-α,PRF1)的CD45RA+CCR7-TE CAR-T细胞比例显著较高,并且表达趋化因子(CCL3、CCL4 和 CCL5)的细胞比例有增加的趋势(图5H)。
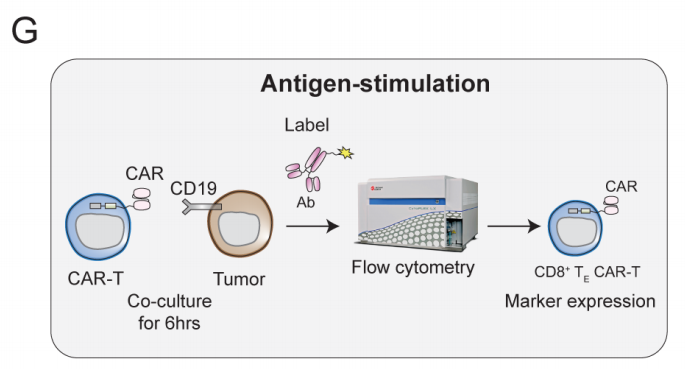
图5G 与CD19+肿瘤细胞共培养后评估标记物表达的实验设置图

图5H 与CD19+肿瘤细胞共培养后,缓解者(R;n=8)和未缓解者(NR;n=14)的CD8+
TE CAR-T细胞表达IFN-γ、TNF-α、PRF1、GZMB、CCL3、CCL4和CCL5的比例
总之,缓解者的CAR-T细胞输注产品具有更多的CD8+ TE CAR-T细胞,并且在抗原刺激(与肿瘤细胞共培养)后,这些细胞中表达效应分子IFN-γ和TNF-α的比例增高。此外,抗原刺激后,与未缓解者相比,缓解者的CAR-T细胞上CD27表达更高,CD25表达更低。
研究结论
研究结果表明,在CAR-T制备过程中,较短的体外扩增时间有利于产生更多的效应CD8+ CAR-T细胞。此外,在CAR-T输注产品中,高多功能指数、高细胞毒性和细胞因子分泌特征/表型以及低功能障碍表型的CD8+ CAR-T细胞与CAR-T治疗的临床缓解相关。
免责声明:本资料为专业医学资料,旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参考;任何处方请参考产品最新详细处方资料。本文件可能包含涉及医学情况、健康及治疗方法的信息。相关信息不得用作诊断或治疗,不能替代专业医学意见。
审批编号:NP-NHL-2023.12-29 valid until 2025.12
供稿与审核:临床开发与医学部
推荐阅读
-
【2023 ASH】ZUMA-1研究6年随访生存数据:Axi-cel点亮难治性LBCL治愈之光
-
【2023 ASH】Axi-cel治疗LBCL:二线 vs 三线,早用更获益
-
【2023 ASH】CAR-T二线治疗R/R LBCL的真实世界证据
-
【2023 ASH】ZUMA-12的3年随访分析展示Axi-cel在一线高危LBCL患者治疗中的风采
-
【2023 ASH】阿基仑赛治疗R/R NHL中国真实世界研究中期分析
-
【2023 ASH】真实世界中Axi-cel治疗LBCL患者的5年随访结局彰显治愈希望
-
【2023 ASH】Brexu-cel治疗R/R B-ALL成人患者的真实世界证据
-
【2023ASH】Brexu-cel治疗高危R/R MCL患者的真实世界结局
-
【2023 ASH】CAR-T之声:一文速览Brexul-cel相关研究的最新进展
-
【ASH 2023】CAR-T细胞治疗重塑DLBCL患者的生存趋势
-
【2023 ASH】CAR-T之声:一文速览Axi-cel相关研究的最新进展
-
CAR-T细胞治疗合并肾功能减退的LBCL患者的真实世界结局
-
临床前研究提示来那度胺可改善第三代CD19 CAR-T细胞对DLBCL的疗效
-
【2023 ESMO】治疗3L+ R/R LBCL,Axi-cel vs Glofit,孰优孰劣?
-
Yescarta®全球上市6周年,为淋巴瘤患者点亮治愈的希望之光
-
奕凯达治疗R/R NHL继中国真实世界研究中期分析数据后再添亚裔人群证据,赵维莅等教授评论文章NEJM新发布!
-
CAR-T细胞治疗R/R LBCL的不良预后因素:欧洲 vs 美国患者
-
CAR-T治疗B-NHL的安全性和有效性不受合并自身免疫性风湿性疾病的影响
-
ctDNA可提高Axi-cel治疗R/R LBCL后PET的特异性
-
有效的桥接疗法可改善CAR-T治疗R/R LBCL患者的临床结局
-
ZUMA-1研究5年随访数据尽显Axi-cel风采,R/R LBCL治愈未来可期
-
真实世界中白细胞单采至输注时间对接受Axi-cel治疗R/R LBCL患者结局的影响
-
Axi-cel用于桥接治疗后达到完全代谢缓解的R/R LBCL患者的结局
-
【2023EHA】Axi-cel与其他CAR-T产品治疗R/R LBCL的白细胞单采至输注时间:一项系统性综述与荟萃分析
-
【2023EHA】早期Pola桥接CD19 CAR-T细胞治疗是改善复发难治B细胞淋巴瘤患者生存的有效策略

