【2023 ASH】真实世界证据:CAR-T治疗R/R LBCL获益不受高龄影响
2023年第65届美国血液学会(ASH)年会于美国东部时间12月9日至12日在San Diego举行。ASH年会是全球血液学领域的国际盛会,本届大会汇集了各国知名血液病学专家最新的重要研究成果,已经公布7,000余篇已接受的摘要,其中CAR-T治疗相关摘要超470篇[1]。
嵌合抗原受体T细胞(CAR-T)治疗是一种备受期待的新型肿瘤免疫治疗方法,具有潜在的治愈能力。目前CAR-T疗法的出现改变了大B细胞淋巴瘤(LBCL) 的治疗模式,而真实世界中接受CAR-T治疗的老年患者的结局报道有限[2]。
在诸多摘要中,小编节选了一篇“一项多中心研究”(Abstract #311),让我们一睹CAR-T治疗老年复发性或难治性LBCL患者的疗效和安全性结果。
摘要编号:311
英文标题:Chimeric Antigen Receptor T-Cell Therapy in Elderly Patients with Relapsed or Refractory Large B-Cell Lymphoma: A Multicenter Study[3]
中文标题:CAR-T治疗老年复发性或难治性大B细胞淋巴瘤患者: 一项多中心研究
研究背景
CAR-T疗法在复发或难治性大B细胞淋巴瘤(R/R LBCL)中显示出治愈潜力。但关键注册临床研究中年龄≥65岁的患者数量有限:ZUMA-1、JULIET和TRANSCEND NHL001研究-2中年龄≥65岁的患者分别占24%、23%和42%。此外,关键注册临床研究和真实世界研究中≥65岁患者的疗效和安全性数据也很有限,但表现出一致的结论:ZUMA-1[4]、CIBMTR[7]和MSKCC[8]研究结果显示,CAR-T治疗在≥65岁患者中的疗效及安全性与<65岁患者的相当。 本研究旨在评估真实世界中CAR-T治疗老年R/R LBCL患者的疗效和安全性。
研究方法
本研究[3]是一项多中心回顾性研究,纳入美国7个中心接受商业CAR-T输注的老年R/R LBCL患者。排除既往接受CAR-T治疗的其他类型淋巴瘤患者(包括套细胞淋巴瘤、滤泡性淋巴瘤等),以及在临床试验中接受过CAR-T治疗的患者。主要终点为PFS、OS、客观缓解率(ORR)和完全缓解(CR)率、不良事件的发生率、性质和严重程度。
使用描述性统计评估基线状态、治疗、缓解和不良事件;使用Kaplan-Meier方法估计时间-事件(Time to event);使用对数秩检验和Cox比例风险模型确定生存期和特征变量的相关性;分类变量的差异统计使用卡方检验。
研究结果
患者基线特征
患者基线特征见表1。共纳入226例患者,输注CAR-T时的中位年龄为71岁(范围65-89),26例(12%)患者≥80岁。143例(63%)为男性,27例(13%)美国东部肿瘤协作组体能状态评分(ECOG PS)≥2。中位造血干细胞移植合并症指数(HCT-CI)为1(范围0-6), 45例(22%)患者HCT-CI评分≥3。163例(72%)为弥漫性大B细胞淋巴瘤(DLBCL),39例(17%)为转化性惰性淋巴瘤,24例(11%)为高级别淋巴瘤(HGBL)。23例(19%)存在大包块病变,177例(82%)为III-IV期,146例(71%)结外部位受累。110例(51%)在CAR-T治疗前乳酸脱氢酶(LDH)升高,既往中位治疗线数为2(范围1-8),104例(46%)既往接受>2线治疗,45例(22%)既往使用过苯达莫司汀,47例(21%)既往接受过干细胞移植。
表1 患者基线特征

桥接治疗方式及缓解情况
117例患者接受桥接治疗:其中71例(61%)接受化疗和/或CD20单克隆抗体(mAb),3例(3%)接受CD20 mAb和/或类固醇,9例(8%)接受来那度胺治疗方案,7例接受CD20抗体和/或皮质类固醇治疗。4例(3%)仅接受类固醇治疗,22例(19%)仅接受放疗。8例(7%)接受放疗联合化疗和/或CD20 mAb。桥接治疗后6例(8%)达到CR,23例(29%)达到部分缓解(PR),17例(22%)患者疾病稳定(SD),32例(41%)出现疾病进展。39例患者未接受评估。
不良事件
不良事件及处理方式见表2。169例(75%)患者发生细胞因子释放综合征(CRS),16例(7%)为3-4级CRS,中位发病时间为3(0-24)天,中位持续时间为4(1-26)天;117例(52%)患者发生免疫效应细胞相关神经毒性综合征(ICANS),59例(26%)为3-4级ICANS,中位发病时间为6(0-24)天,中位持续时间为6(1-90)天。CRS和ICANS的治疗包括托珠单抗(126例[56%])、其他生物制剂(10例[4%])和皮质类固醇(106例[47%])。其他不良事件见表3。
表2 不良事件及处理方式

表3 其他不良事件
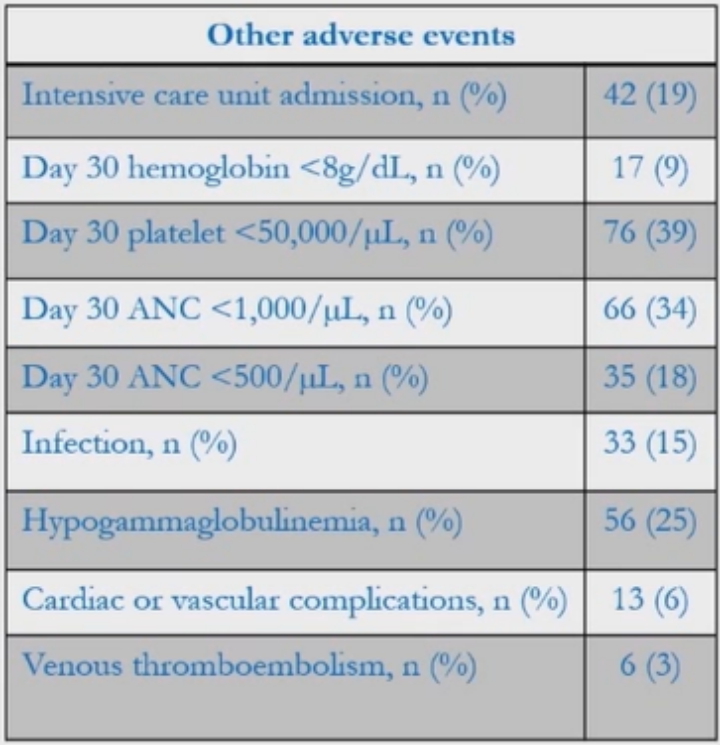
CAR-T治疗的缓解情况
在211例患者中评估CAR-T治疗的缓解情况。第30天的ORR为83%(n=175),最佳ORR为86%(n=181);第30天的CR率为50%(n=106),最佳CR率为62%(n=131);第30天的PR率为33%(n=70),最佳PR率为24%(n=50)(表4)。单因素分析结果显示,ECOG PS≥2、存在大包块病变(≥7cm)、LDH升高和需要桥接治疗与较差的ORR和CR率相关(表5)。
表4 CAR-T治疗的缓解情况
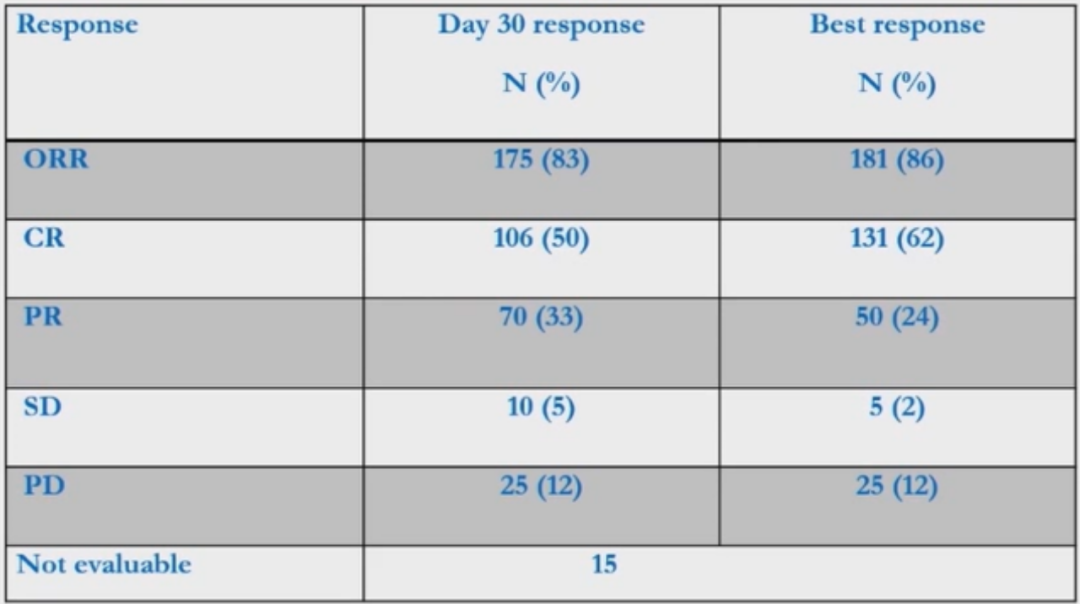
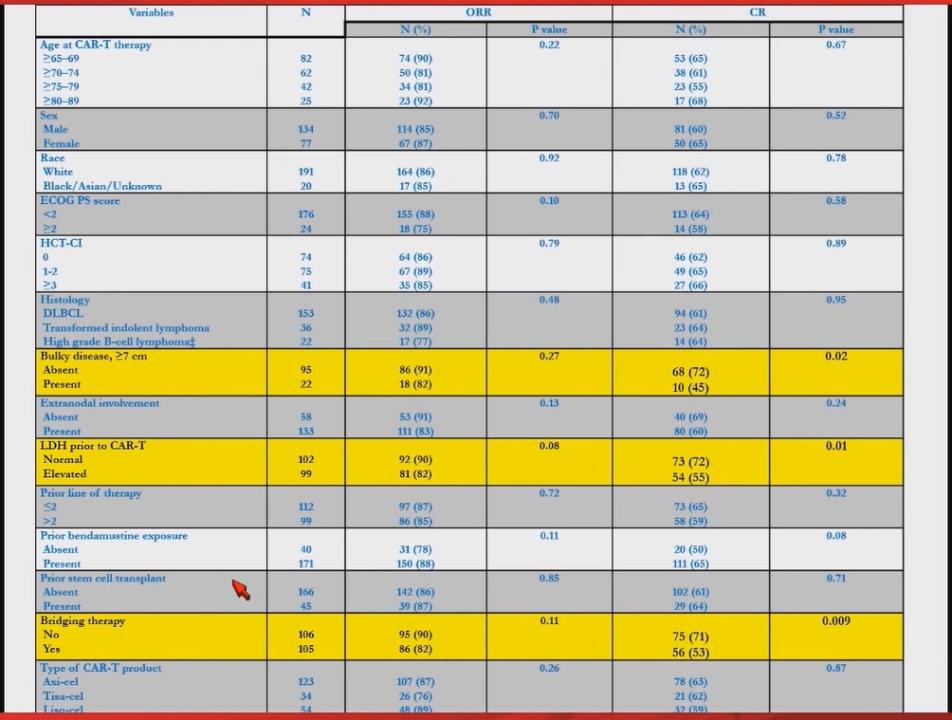
表5 单因素分析显示的与ORR和CR相关的变量
生存获益
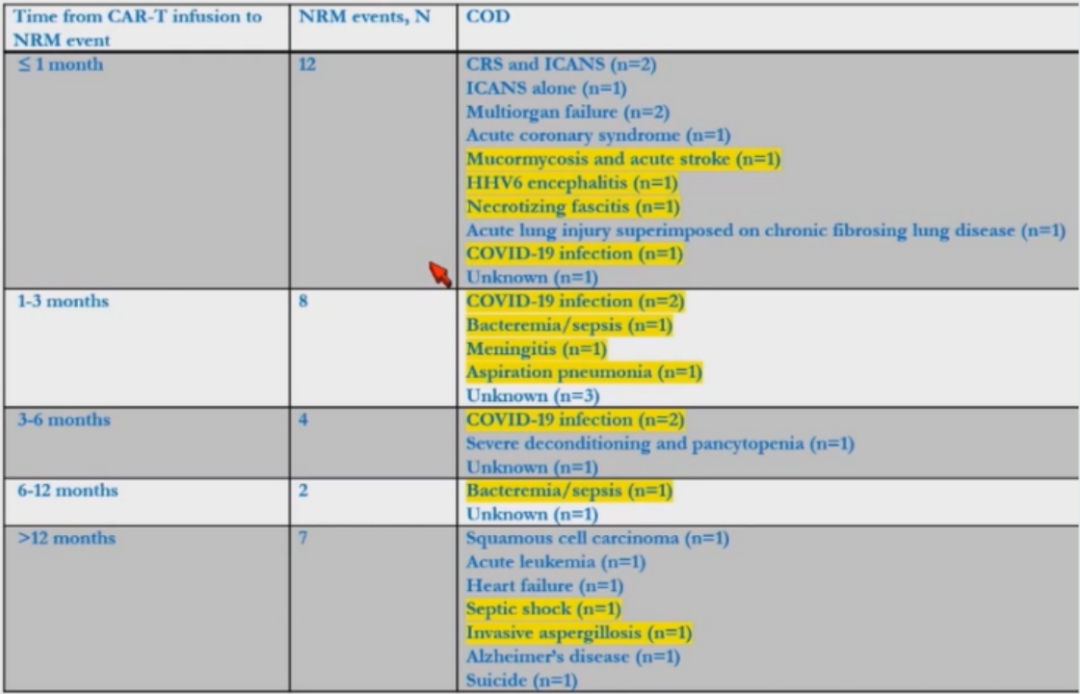
回输后中位随访18.3个月,中位缓解持续时间(DOR)为13.0个月,12个月的DOR率为53%(图1);中位PFS为6.9个月,12个月的PFS率为44%(图2);中位OS为19.1个月,12个月的OS率为61%(图3);1年的复发或进展率为44.4%,1年的非复发死亡率(NRM)为5.3%(图4)。患者NRM事件相关死亡原因见表6。
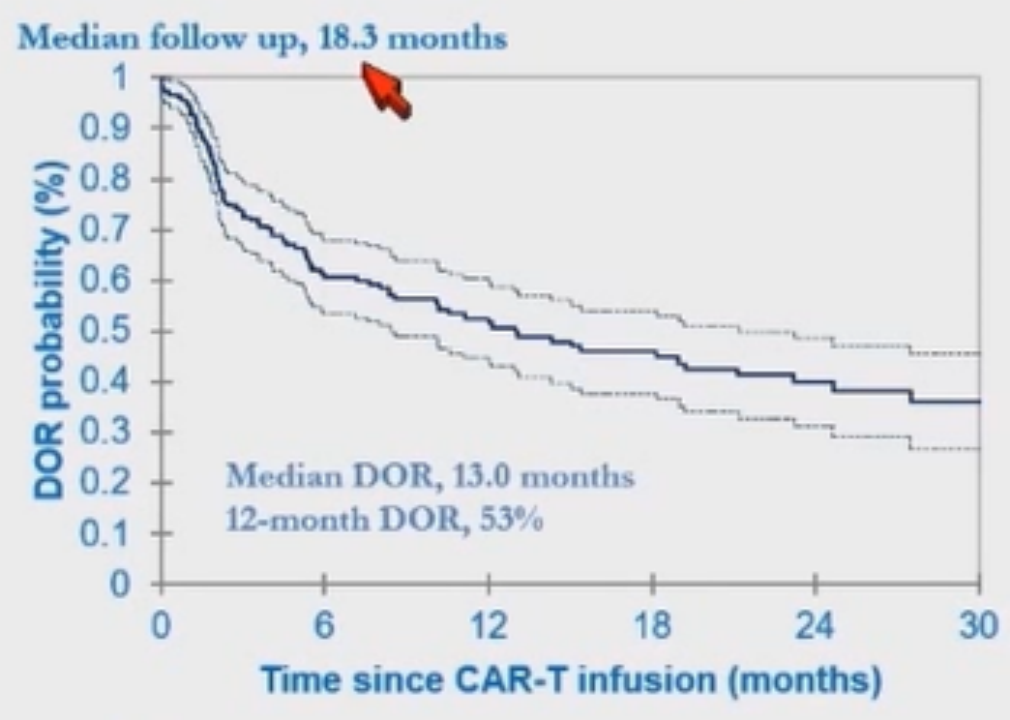
图1 CAR-T输注后的DOR

图2 CAR-T输注后的PFS

图3 CAR-T输注后的OS
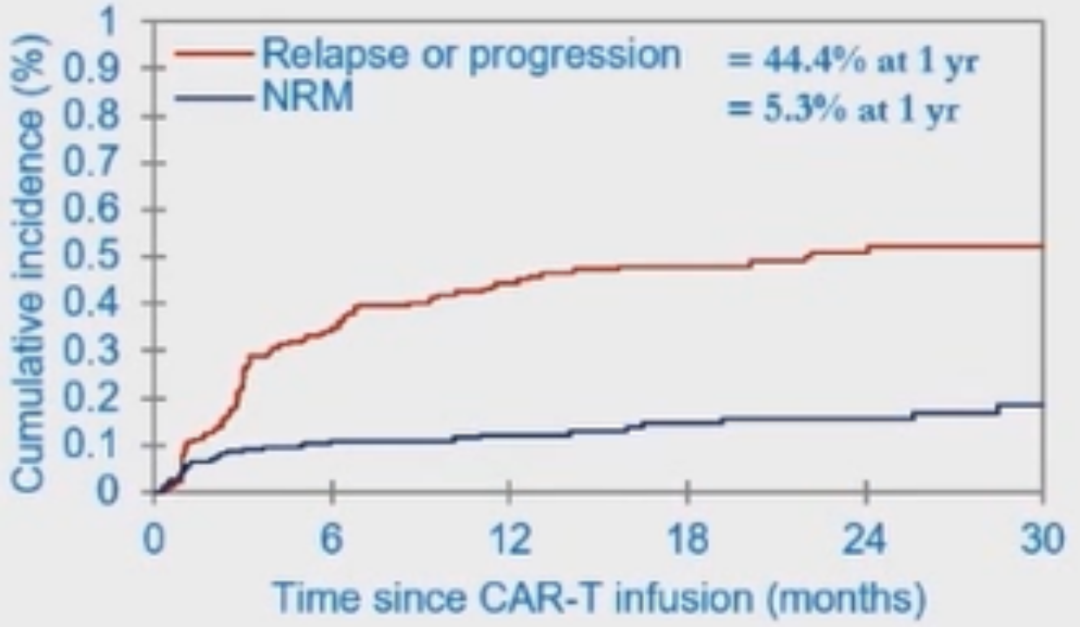
图4 CAR-T输注后的复发/进展率和NRM
表5 患者NRM事件相关死亡原因
不同年龄组患者(年龄≥65-69、年龄≥70-74、年龄≥75-79、年龄≥80-89)的PFS率(P=0.99)和OS率(P=0.73)均无显著差异(图5,图6)。
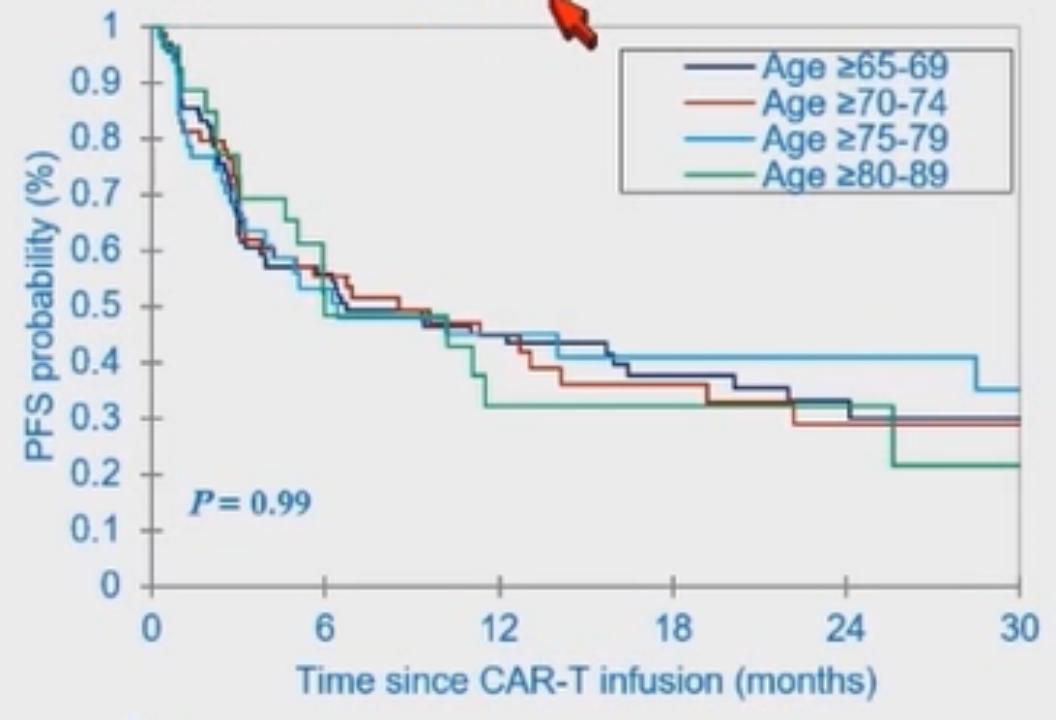
图5 不同年龄组患者的PFS

图6 不同年龄组患者的OS
患者接受不同CAR-T产品输注的PFS率(Axi-cel VS Tisa-cel VS Liso-cel:P=0.28)和OS率(Axi-cel VS Tisa-cel:P=0.32)均无显著差异(图7,图8)。
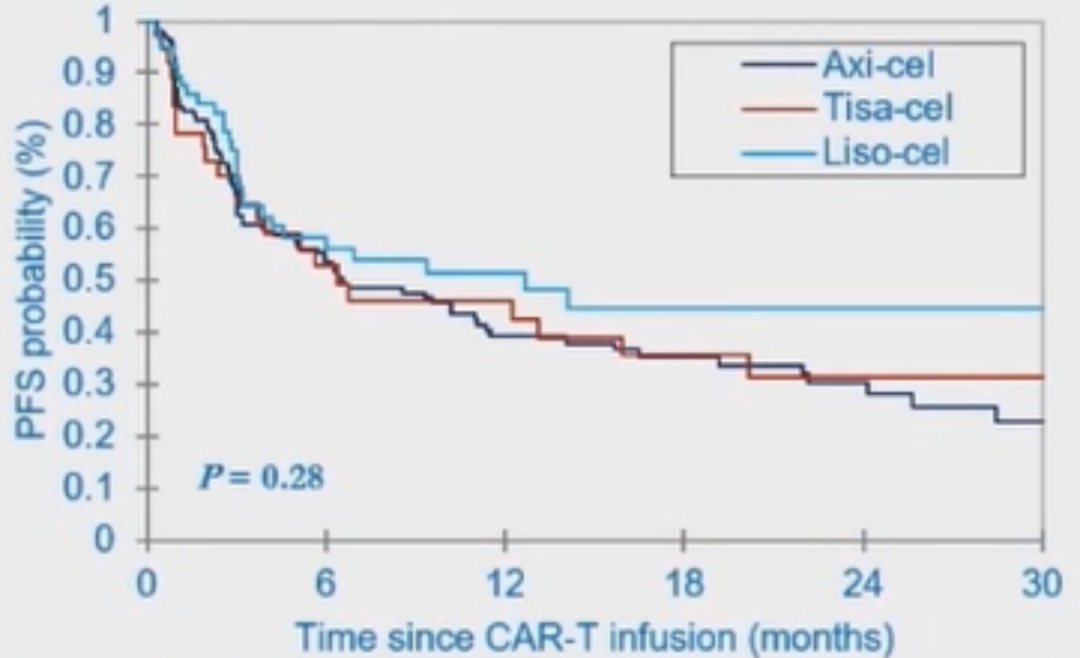
图7 不同CAR-T产品组患者的PFS
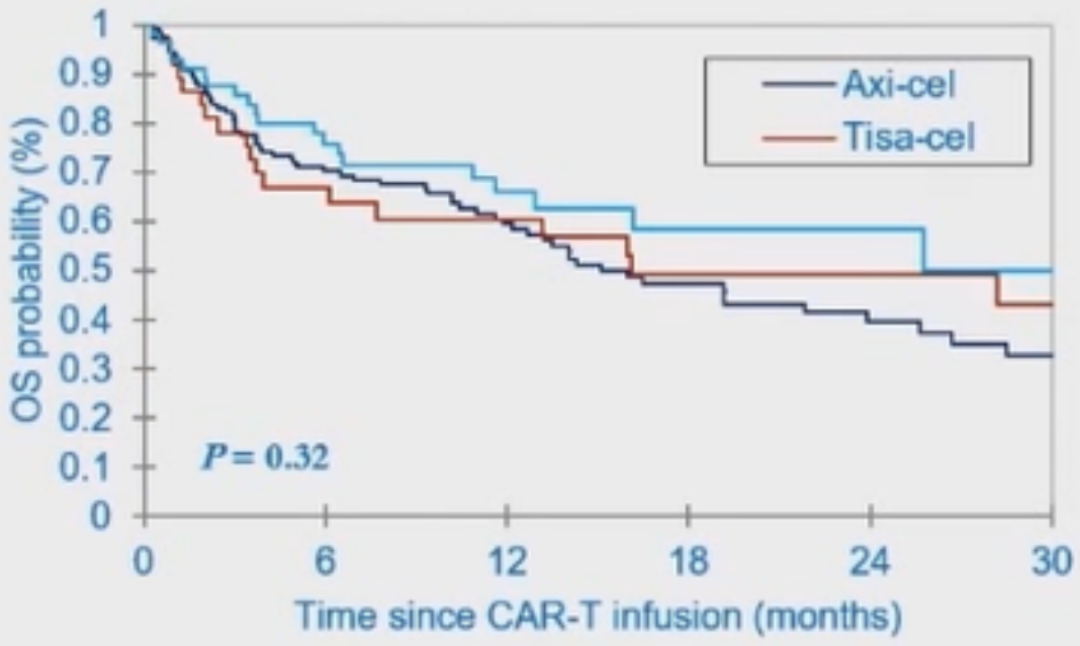
图8 不同CAR-T产品组患者的OS
与ECOG PS≥2的患者相比,ECOG PS<2患者的PFS率(P=0.04)和OS率(P=0.005)显著更好(图9,图10)。
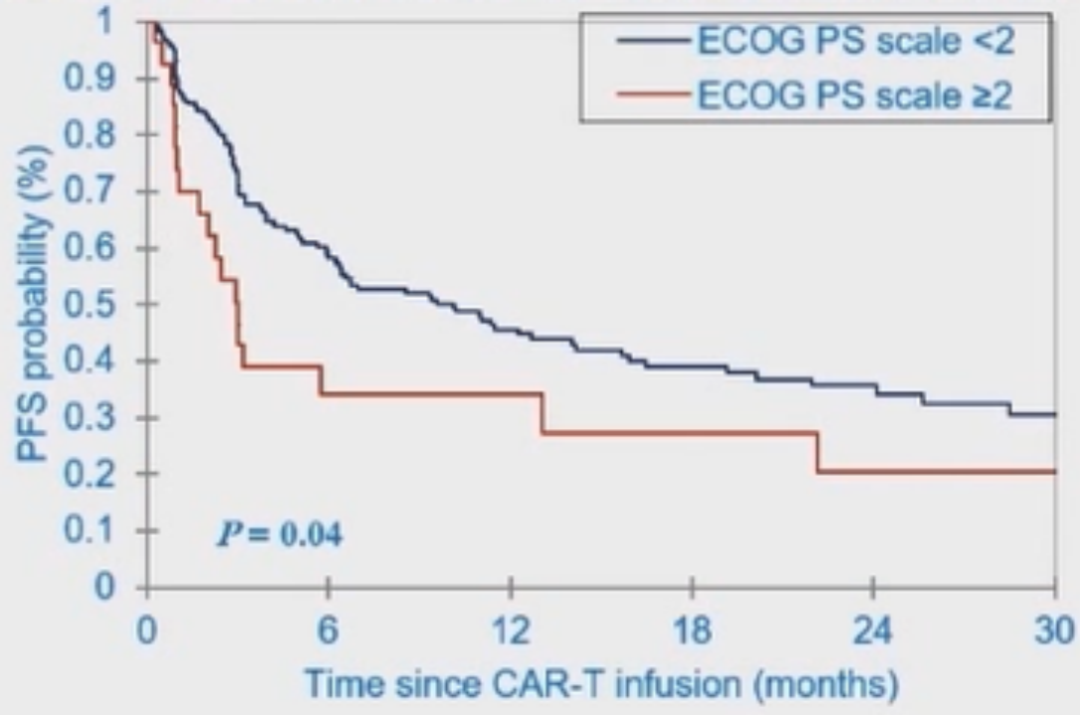
图9 根据ECOG PS分组的PFS
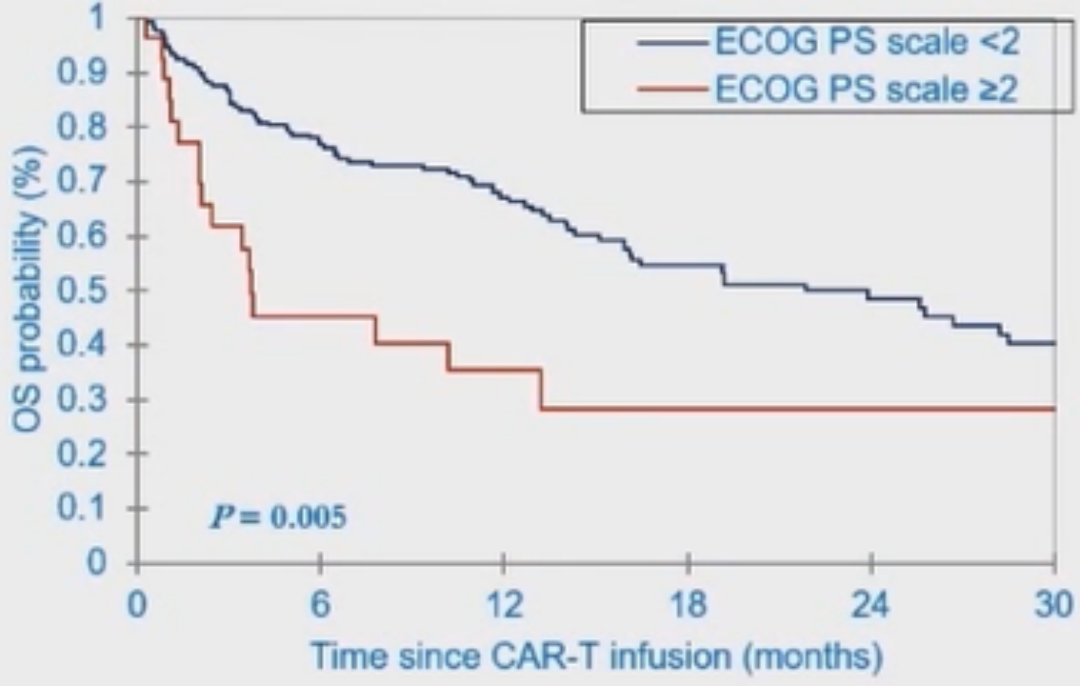
图10 根据ECOG PS分组的OS
不同HCT-Cl评分组(HCT-Cl评分为0、HCT-Cl评分为1-2、HCT-Cl评分≥3)患者的PFS率(P=0.54)和OS率(P=0.14)无显著差异(图11、图12)。
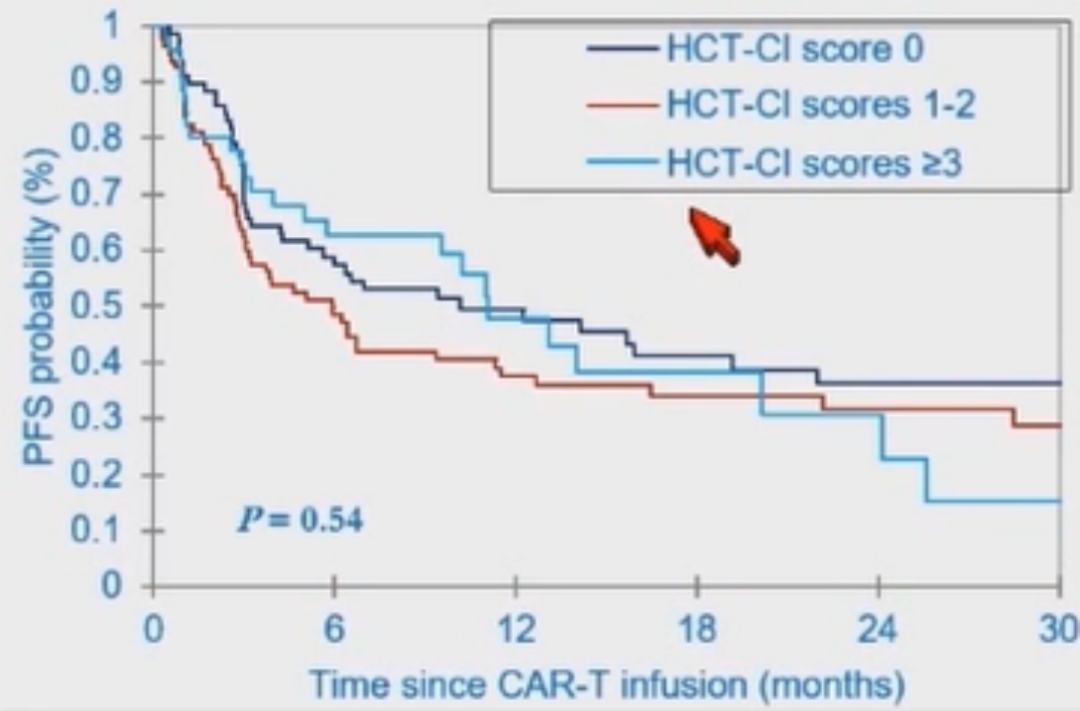
图11 不同HCT-Cl评分组患者的PFS
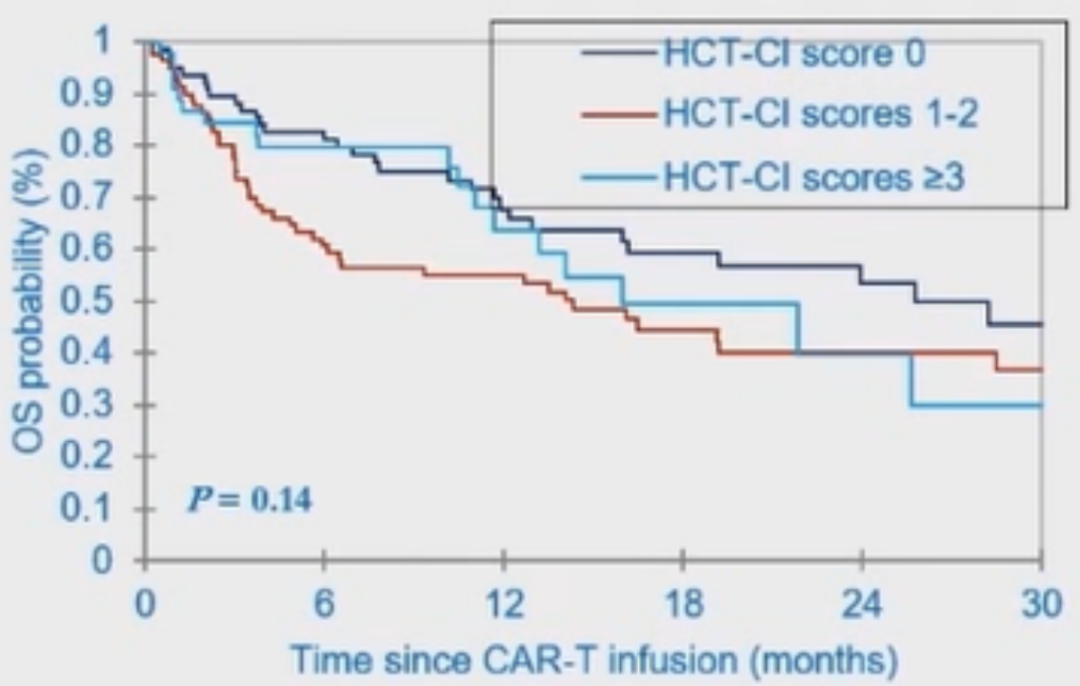
图12 不同HCT-Cl评分组患者的OS
与存在大包块病变的患者相比,不存在大包块病变的患者的PFS率显著更好(P=0.02)(图13)。与III-IV期患者相比,I-II期患者的PFS率显著更好(P=0.01)(图14)。与存在结外受累患者相比,无结外受累患者的PFS率显著更好(P=0.03)(图15)。与LDH升高患者相比,LDH未升高患者的PFS率显著更好(P=0.005)(图16)。
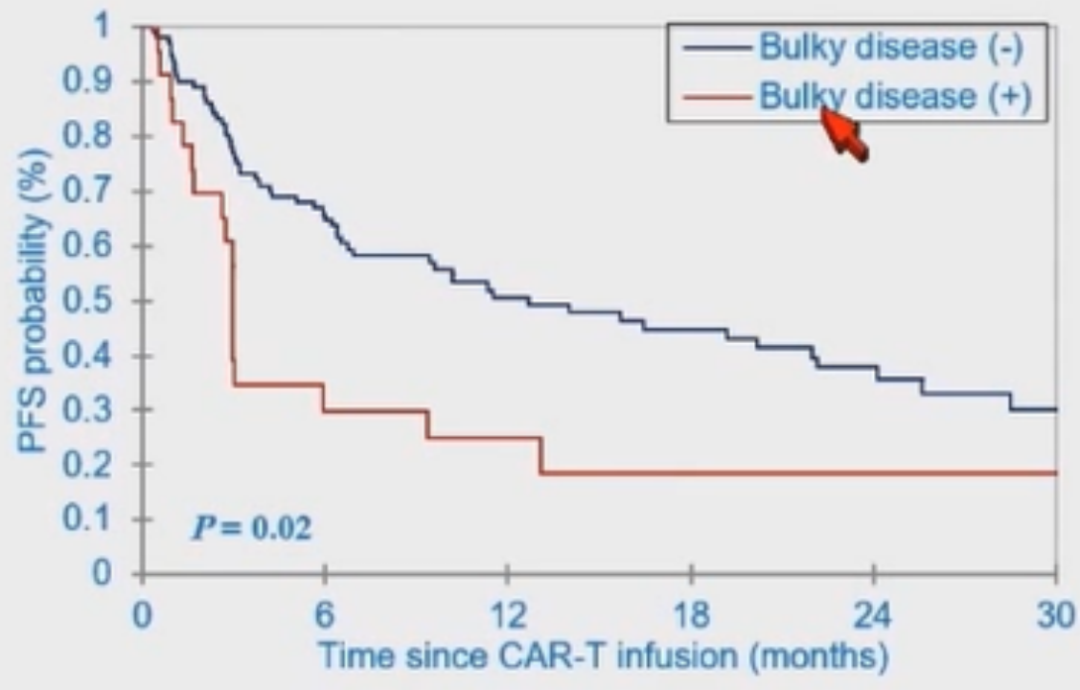
图13 大包块与无大包块患者的PFS
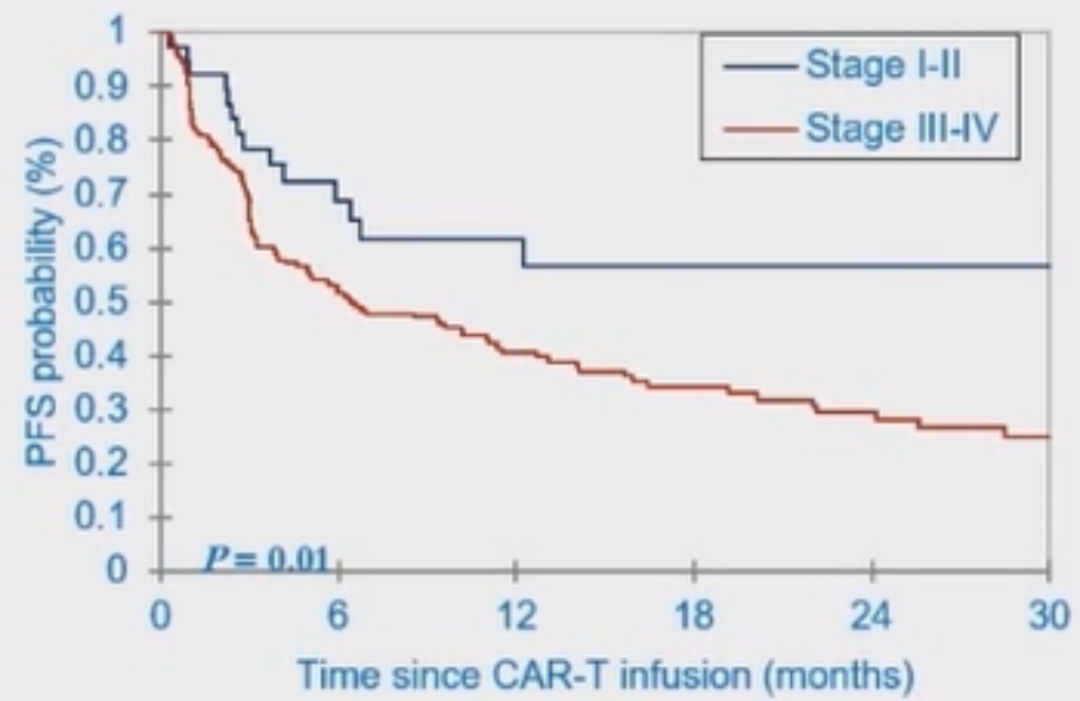
图14 不同分期患者的PFS
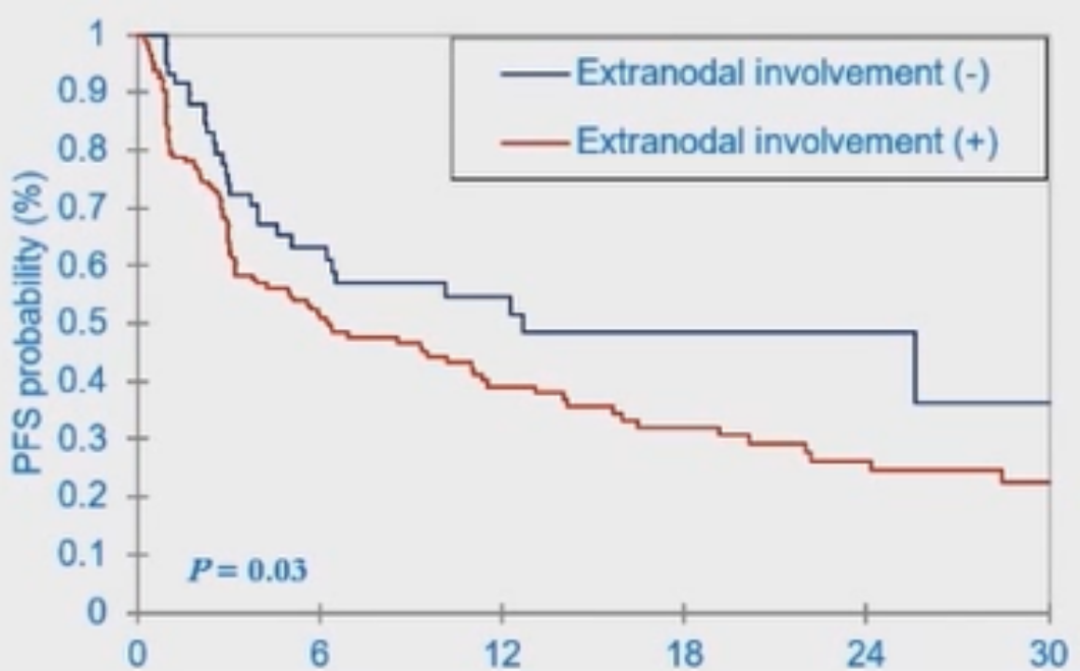
图15 不同结外受累状态患者的PFS
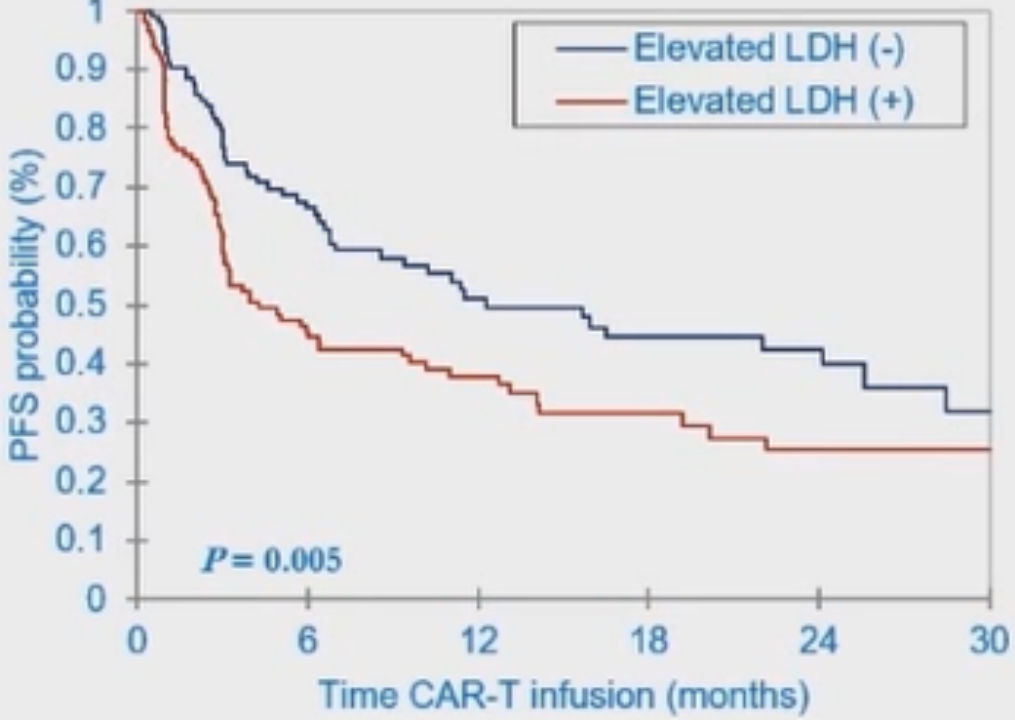
图16 不同LDH水平患者的PFS
CAR-T治疗后复发的挽救治疗
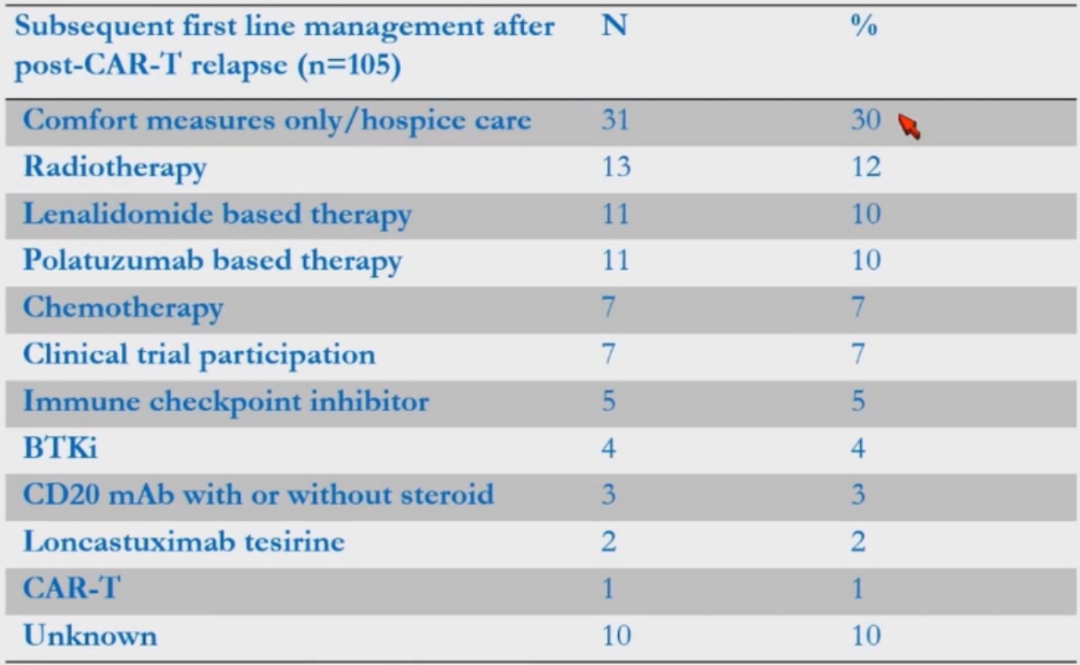
105例患者在CAR-T治疗后复发并接受了挽救治疗,其中31例(30%)仅采取姑息治疗/临终关怀,13例(12%)接受放疗,11例(10%)接受来那度胺方案,11例(10%)接受维泊妥珠单抗方案,7例(7%)接受化疗,7例(7%)参加临床试验,5例(5%)接受免疫抑制剂,4例(4%)接受布鲁顿酪氨酸激酶抑制剂(BTKi),3例(3%)接受CD20 mAb和/或类固醇,2例(2%)接受Loncastuximab tesirinc,1例(1%)接受CAR-T治疗(表6)。
表6 CAR-T治疗后复发的挽救治疗
研究结论
本项多中心研究显示,真实世界中CAR-T治疗的疗效和安全性结果与关键注册临床试验相当。无论患者年龄如何,≥3级CRS和 ICANS的发生率相当,但≥3级ICANS发生率受ECOG PS、LDH和CAR-T产品类型影响。
无论患者年龄(包括≥80岁的患者)和使用的CAR-T产品类型如何,生存结果均相当。与年轻患者相似,老年患者中高肿瘤负荷和CAR-T输注时较差的体能状态与不良生存预后相关。CAR-T治疗不应仅因年龄而将老年患者排除在外,CAR-T治疗获益不受年龄影响。
免责声明:本资料为专业医学资料,旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参考;任何处方请参考产品最新详细处方资料。本文件可能包含涉及医学情况、健康及治疗方法的信息。相关信息不得用作诊断或治疗,不能替代专业医学意见。
审批编号:NP-NHL-Axi-Cel-2024.1-19 valid until 2026.1
供稿与审核:临床开发与医学部
推荐阅读
-
【2023 ASH】CAR-T治疗显著改善双打击/三打击淋巴瘤患者生存:早用更获益
-
【2023 ASH】CIBMTR真实世界证据:桥接治疗对Axi-cel治疗R/R LBCL的影响
-
单细胞RNA分析表明第三代CAR-T细胞的内在功能特征与淋巴瘤疗效相关
-
【2023 ASH】ZUMA-1研究6年随访生存数据:Axi-cel点亮难治性LBCL治愈之光
-
【2023 ASH】Axi-cel治疗LBCL:二线 vs 三线,早用更获益
-
【2023 ASH】CAR-T二线治疗R/R LBCL的真实世界证据
-
【2023 ASH】ZUMA-12的3年随访分析展示Axi-cel在一线高危LBCL患者治疗中的风采
-
【2023 ASH】真实世界中Axi-cel治疗LBCL患者的5年随访结局彰显治愈希望
-
【2023 ASH】Brexu-cel治疗R/R B-ALL成人患者的真实世界证据
-
【2023 ASH】CAR-T之声:一文速览Brexul-cel相关研究的最新进展
-
【ASH 2023】CAR-T细胞治疗重塑DLBCL患者的生存趋势
-
【2023 ASH】CAR-T之声:一文速览Axi-cel相关研究的最新进展
-
CAR-T细胞治疗合并肾功能减退的LBCL患者的真实世界结局
-
临床前研究提示来那度胺可改善第三代CD19 CAR-T细胞对DLBCL的疗效
-
【2023 ESMO】治疗3L+ R/R LBCL,Axi-cel vs Glofit,孰优孰劣?
-
Yescarta®全球上市6周年,为淋巴瘤患者点亮治愈的希望之光
-
奕凯达治疗R/R NHL继中国真实世界研究中期分析数据后再添亚裔人群证据,赵维莅等教授评论文章NEJM新发布!
-
CAR-T细胞治疗R/R LBCL的不良预后因素:欧洲 vs 美国患者
-
CAR-T治疗B-NHL的安全性和有效性不受合并自身免疫性风湿性疾病的影响
-
ctDNA可提高Axi-cel治疗R/R LBCL后PET的特异性
-
有效的桥接疗法可改善CAR-T治疗R/R LBCL患者的临床结局

