CAR-T细胞疗法相关AE的预防策略和安全性管理
嵌合抗原受体T(CAR-T)细胞疗法是一种通过基因工程技术把CAR结构修饰于患者自身T细胞,然后回输至患者体内,以实现抗肿瘤效应的免疫治疗手段[1,2]。随着CAR-T细胞疗法的临床应用逐渐增多,相关不良事件(AE)受到了越来越多的关注,其中细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)是最受关注的并发症[3]。早期预防用药、密切监测以及对症治疗可有效降低和缓解AE,给患者带来更大的临床获益。
1. 预防性用药的合理应用
根据患者的具体情况和风险评估,可采取针对性预防措施。研究表明,高肿瘤负荷患者接受CAR-T细胞回输前或回输早期给予肿瘤坏死因子-α(TNF-α)抑制剂、Janus激酶(JAK)抑制剂和皮质类固醇等能降低严重CRS和ICANS的发生率[4,5,6]。例如,一项真实世界研究数据显示,预防性使用地塞米松可降低CAR-T细胞治疗非霍奇金淋巴瘤(NHL)后的3-4级神经毒性发生率[5]。需要注意的是,预防性用药可能影响CAR-T细胞功能或增加其他不良反应的风险,因此需谨慎权衡并密切监测。
2. 密切监测的关键措施
CAR-T细胞回输后需密切监测AE。以CRS为例,监测措施包括:每隔2-4 h记录生命体征,每日检测血常规、血细胞计数、凝血功能、C反应蛋白(CRP)、铁蛋白和生化指标等。若条件允许,每2天检测血清IL-6、IL-10和干扰素-γ(IFN-γ)等水平,以及外周血CD19+ B细胞和CD3+ T细胞比例变化[7]。这些监测措施有助于及时发现和处理CAR-T细胞治疗相关的AE,确保治疗的安全性和有效性。
3. CAR-T细胞治疗相关AE的临床特征和治疗
3.1 CRS的临床特征和治疗
CRS是因免疫细胞被激活释放大量细胞因子而引发的严重全身炎症反应[8],发生率为30%-100%,其中≥3级CRS的发生率为10%-30%[9]。CRS通常在CAR-T细胞回输后14天内发生[10],伴随发热、低血压和低氧血症[3]。CRS按症状严重程度分为四个等级,1级可对症降温和补液;≥2级可根据情况使用托珠单抗,效果不佳时可加用激素。具体的治疗措施参考相关指南(表1)[3]。
表1 CRS四个等级的症状和治疗
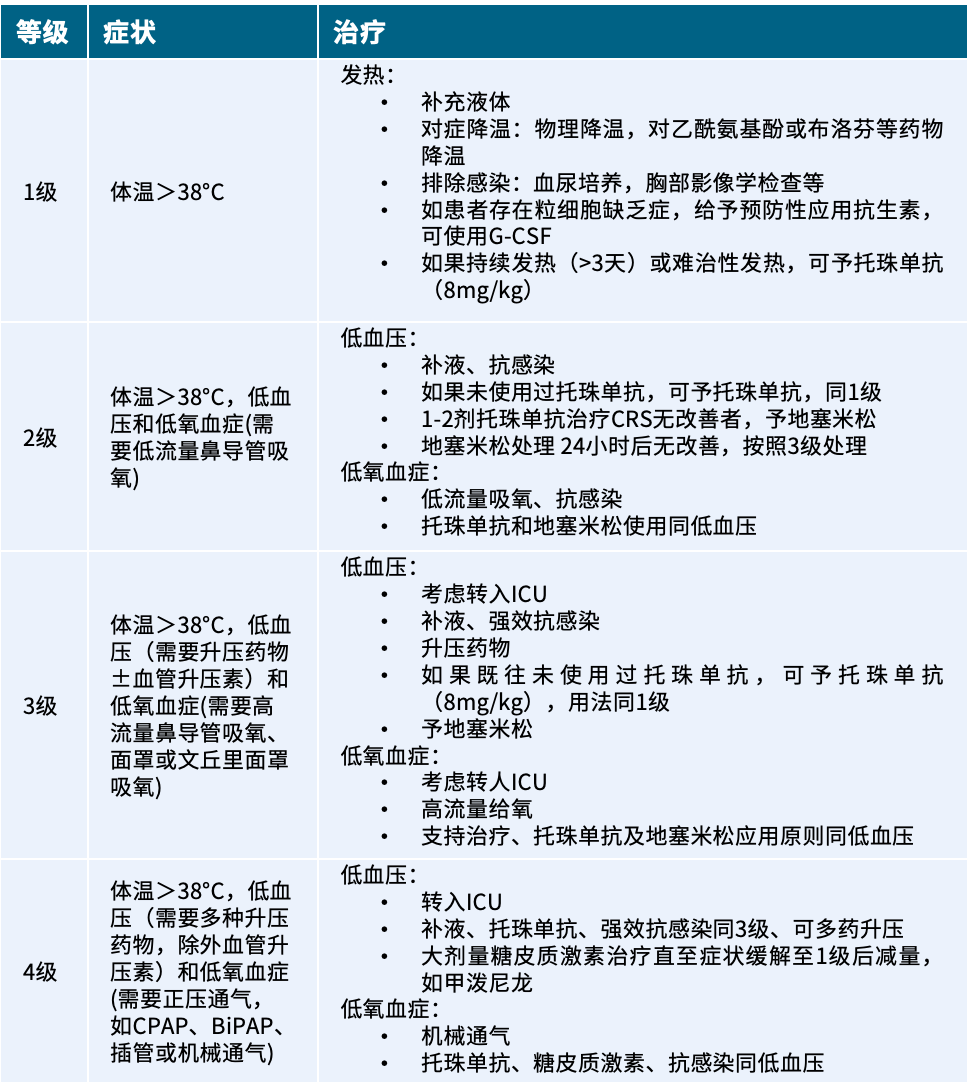
注:CPAP:持续气道正压通气;BiPAP,双水平正压通气;G-CSF:粒细胞集落刺激因子;CRS:细胞因子释放综合征;ICU,重症监护病房。
3.2 ICANS的临床特征和治疗
ICANS是CAR-T细胞等免疫治疗引起的T细胞及其他免疫效应细胞激活,影响CNS的病理过程[11],发生率为20%-60%,其中≥3级ICANS的发生率为12%-30%[12],通常发生于CRS之后[13]。ICANS按症状严重程度分为四个等级,对于1级且合并CRS的患者,可给予托珠单抗;对于≥2级的患者,若托珠单抗效果不佳或未合并CRS,可考虑加用激素。具体的治疗措施参考相关指南(表2)[3]。
表2 ICANS四个等级的症状和治疗
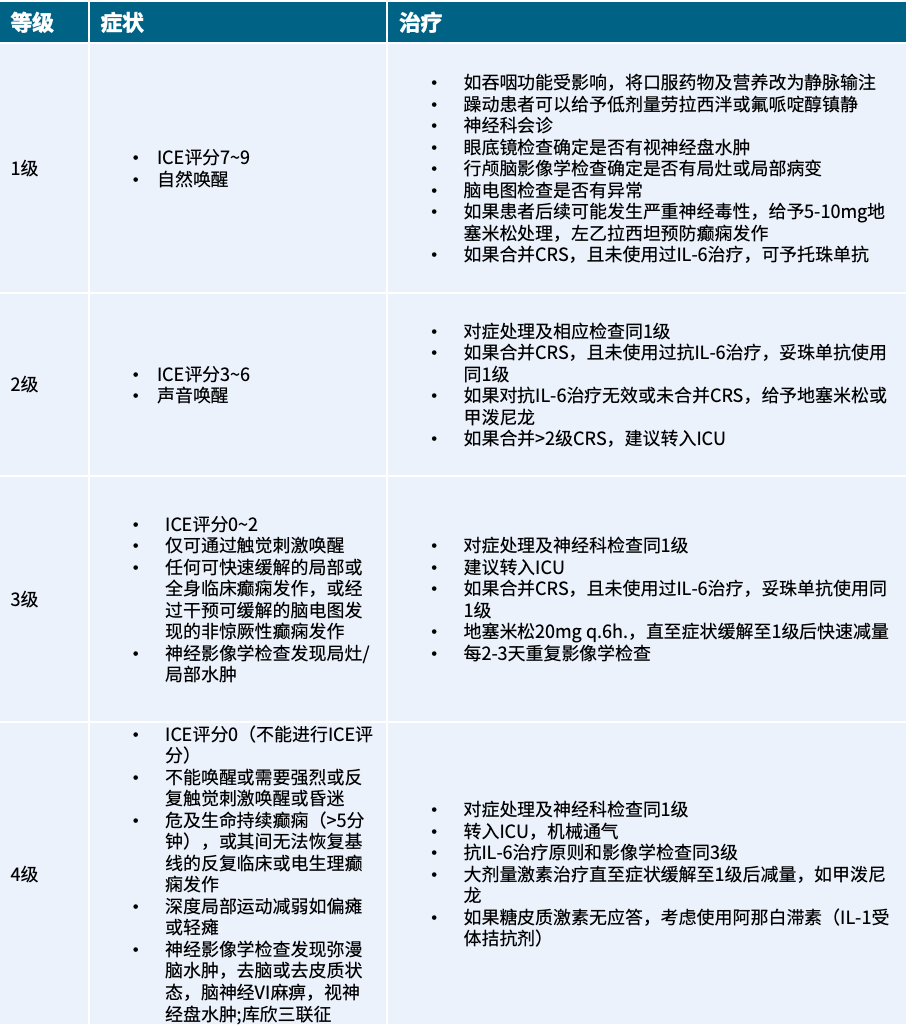
注:ICE,免疫效应细胞相关脑病评分;脑神经VI麻痹:外展神经麻痹;CRS:细胞因子释放综合征;IL-6:白细胞介素-6;q.6h:每6小时一次;ICU,重症监护病房。
3.3 其他可能发生AE的临床特征和治疗
CAR-T细胞回输后还可能出现感染、血小板减少症、B细胞缺乏症/低丙种球蛋白血症、免疫效应细胞相关血液毒性等AE。感染发生率约为55%,其中≥3级的严重感染约为33%,应按照相关指南给予抗感染治疗[3]。对于血小板减少症的患者,当血小板低于20×109/L或观察到出血症状时,应进行血小板回输或给予血小板生成素(TPO)、TPO受体激动剂等治疗[14]。
结 论
CAR-T细胞治疗的相关AE需通过严密监测和快速识别来控制,并采取适当的措施进行管理,这对有效性和安全性之间的平衡至关重要。目前,CAR-T细胞疗法的安全性管理日益完善,在临床应用中的风险得到有效控制,安全性得到提升,门诊给药前景可期[15]。
免责声明:本资料为专业医学资料,旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参考;任何处方请参考产品最新详细处方资料。本文件可能包含涉及医学情况、健康及治疗方法的信息。相关信息不得用作诊断或治疗,不能替代专业医学意见。
审批编号:NP-NHL-Axi-Cel-2024.11-22 valid until 2026.11
供稿与审核:临床开发与医学部

