产品属性对Axi-cel二线治疗LBCL的疗效与安全性影响
全球多中心Ⅲ期随机对照试验ZUMA-7研究已证实,对于复发或难治性大B细胞淋巴瘤(R/R LBCL)患者,与二线标准治疗(SOC)相比,Axicabtagene Ciloleucel(Axi-cel)二线治疗的疗效显著更优,安全性可控[1][2]。
然而,仍有不少患者对嵌合抗原受体T(CAR-T)细胞疗法表现出原发性耐药(无应答)或继发性耐药(初始缓解后复发),因此需要进一步探索CAR-T细胞产品特征和患者特征与治疗耐药和安全性之间的相关性。
本研究分析了ZUMA-7研究中接受Axi-cel治疗患者的临床结局与CAR-T产品的药代动力学、血清药效学以及Axi-cel产品和单采产品属性的关联性[3]。
Filosto S, Vardhanabhuti S, Canales MA, et al. Product Attributes of CAR T-cell Therapy Differentially Associate with Efficacy and Toxicity in Second-line Large B-cell Lymphoma (ZUMA-7). Blood Cancer Discov. 2024;5(1):21-33. doi:10.1158/2643-3230.BCD-23-0112.
-
CAR-T细胞扩增峰值与临床缓解和安全性有关。
-
单采血和最终CAR-T产品中CD27+ CD28+初始T细胞表型(CCR7+ CD45RA+)与增效减毒和较少的既往治疗线数相关。
研究方法
本研究基于两项临床试验(ZUMA-7研究与ZUMA-1研究的队列1与2)的安全性分析集中的可评估样本进行分析。ZUMA-7研究的安全性分析集定义为随机接受≥1剂Axi-cel(目标剂量为2×106 CAR-T细胞/kg,最大目标剂量为2×108 CAR-T细胞)或SOC的患者。ZUMA-1研究的安全性分析集定义为所有接受Axi-cel治疗(任何剂量)的患者。ZUMA-7研究的疗效终点包括无事件生存期(EFS)、无进展生存期(PFS)、客观缓解率(ORR)、最佳缓解、缓解持续时间(DOR)以及持续缓解等,安全性终点包括细胞因子释放综合症(CRS)与神经事件(NE)发生率等。
通过qPCR(实时荧光定量聚合酶链式反应)进行抗CD19 CAR-T细胞的药代动力学分析。在CAR-T细胞制备过程中分析Axi-cel产品的T细胞表型与其他属性。采用流式细胞仪CellCarta进行各表型T细胞的检测[中央记忆T细胞(TCM)、初始T细胞、效应记忆T细胞(TEM)、终末分化效应记忆(TEMRA)T细胞、CD27+ CD28+天然CD4 T细胞、CD27+ CD28+初始CD8 T细胞和CD27+ CD28+初始T细胞等] ,以各表型T细胞数量占总T细胞数量的百分比计算。使用经过验证的Meso Scale Discovery方法(Medpace)分析了29种血清细胞因子、趋化因子和其他炎症标志物。
研究结果
CAR-T细胞扩增与临床结局的相关性
Axi-cel二线治疗的药代动力学特征显示,CAR-T细胞扩增峰值与客观缓解具有直接相关性(图1)。对于持续缓解的患者(n=70)与缓解后出现进展的患者(n=64),两者CAR-T细胞扩增峰值水平相当(图1),且高于原发耐药的患者(n=20)。
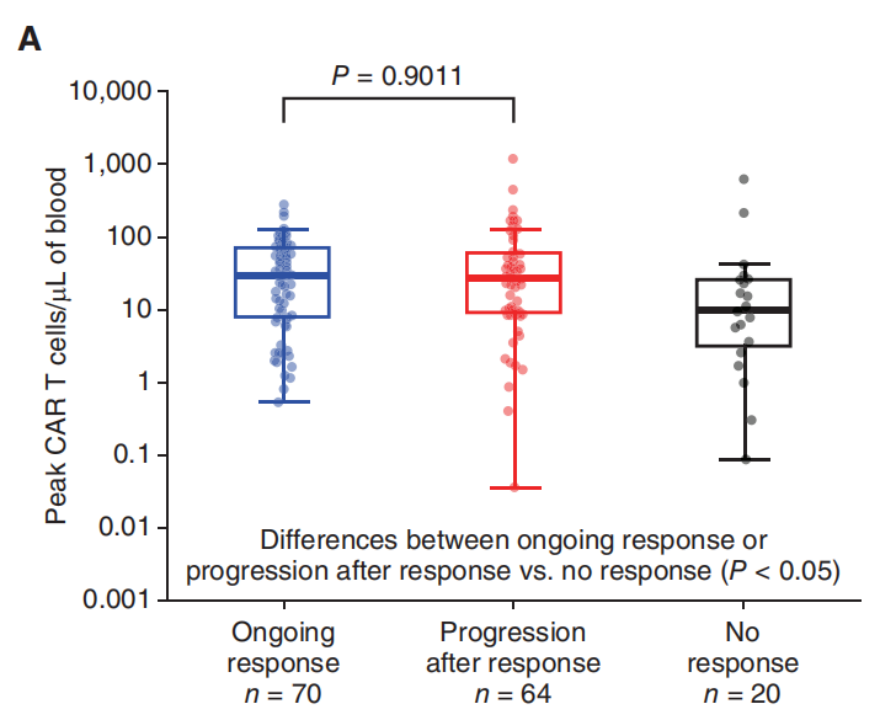
图1 CAR-T细胞扩增峰值与持续缓解、缓解后进展、无缓解患者之间的相关性
CAR-T细胞扩增峰值与≥3级NEs显著相关(p=0.0006),发生≥3级NEs患者(n=33)的中位CAR-T细胞峰值是发生<3级NEs患者(n=129)的2.6倍(图2a)。尽管CAR-T细胞扩增峰值与≥3级CRS无显著相关性(p=0.2040),但发生≥3级CRS患者的中位CAR-T细胞峰值是发生<3级RCS患者的2倍(图2b)。
a
b
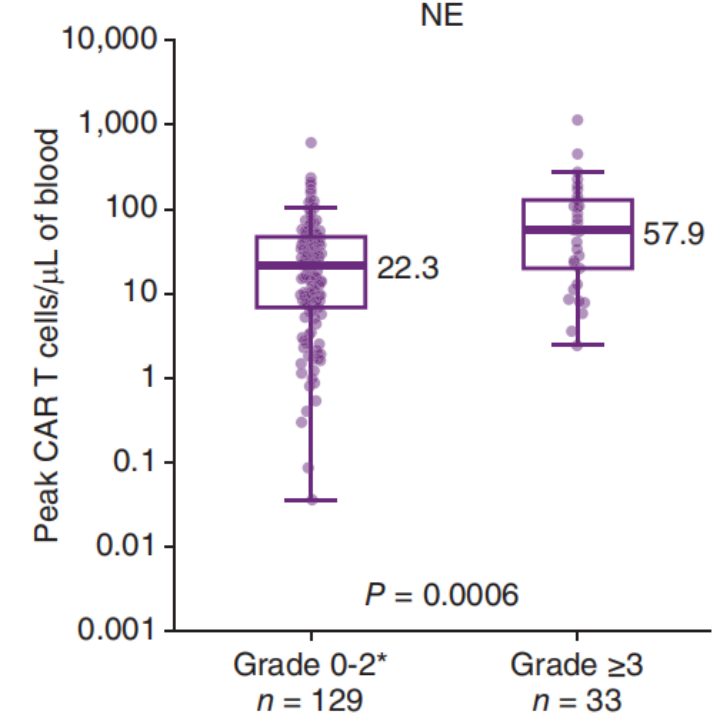
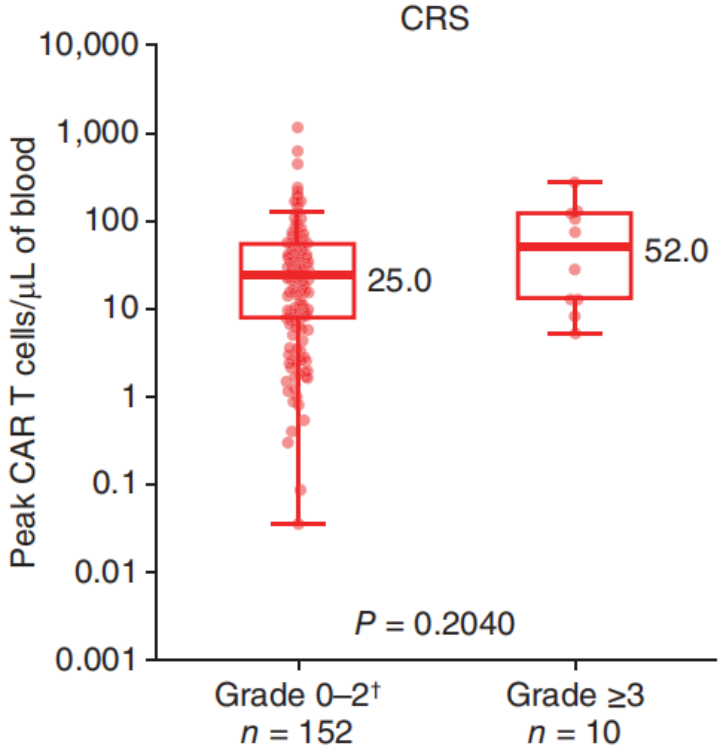
图2 CAR-T细胞扩增峰值与发生≥3级或<3级NEs(a)和CRS(b)之间的相关性
此外,尽管可评估样本量较少(n=45),且检测水平较低,但在CAR-T回输后第3天每μL血液中CAR-T细胞的数量与持续缓解相关(p=0.0439,图3),但与不良事件严重程度无显著相关性(CRS:p=0.48,NE:p=0.56)。
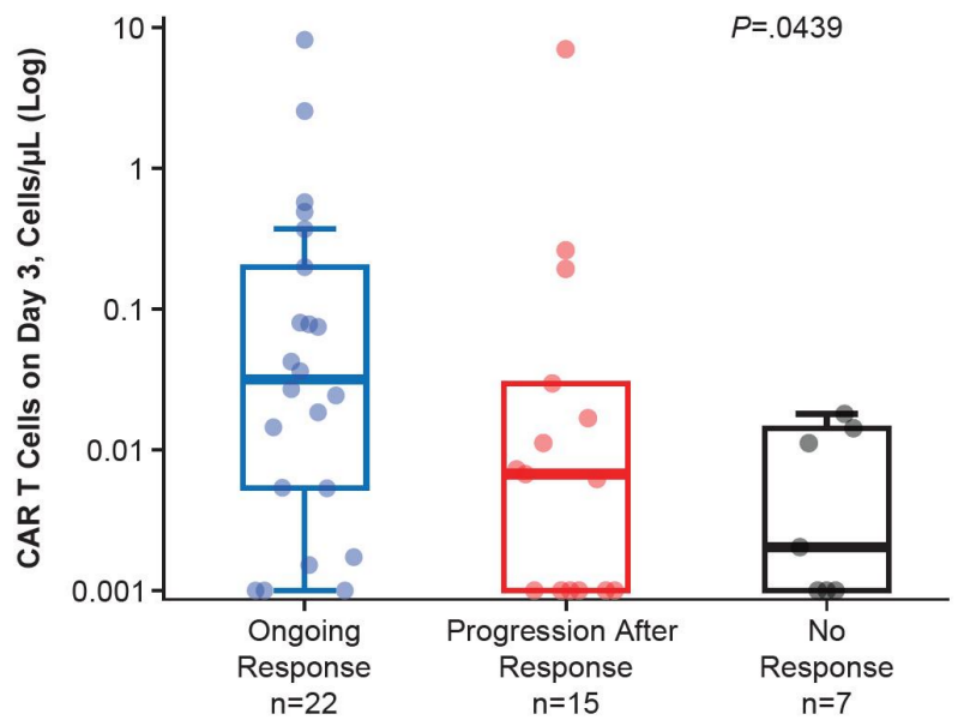
图3 回输后早期(Day 3)CAR-T细胞扩增与持续缓解之间的相关性
Axi-cel产品中的初始T细胞与疗效之间的相关性
初始T细胞占总T细胞的百分比水平(以下简称初始T细胞百分比)与疗效指标呈正相关。与缓解后进展和无缓解的患者相比,持续缓解的患者的初始T细胞百分比水平升高(p=0.0408,图4)。与此同时,初始T细胞百分比水平与EFS的改善显著相关,无论初始T细胞百分比>中位值或≤中位值,Axi-cel治疗的EFS改善程度均优于SOC(p<0.0001,图5)。

图4 在持续缓解、缓解后进展以及无缓解的患者中,初始T细胞占总T细胞的百分比
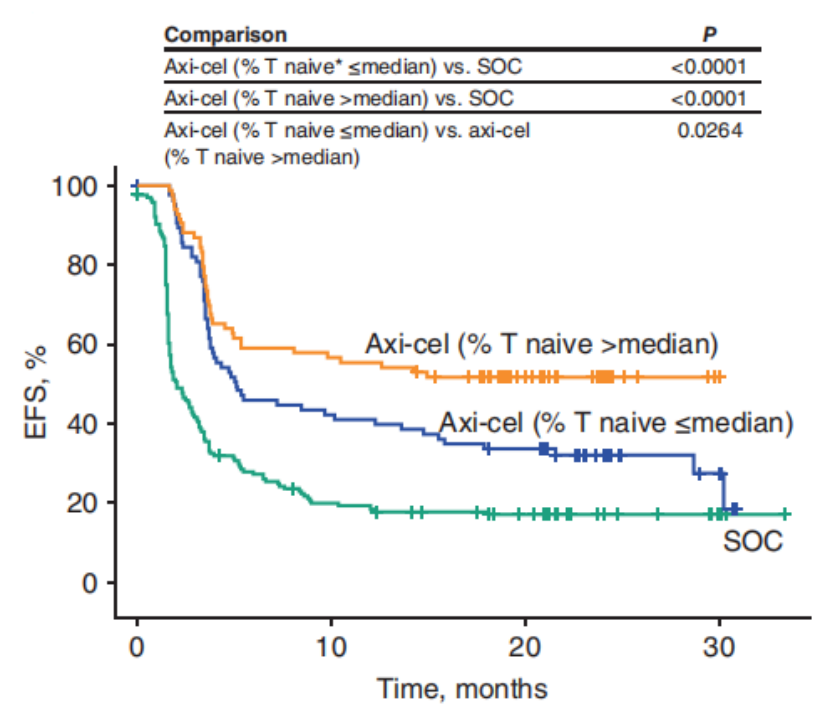
图5 基于初始T细胞百分比中位值(>中位值 vs ≤中位值)和治疗方案(Axi-cel vs SOC)进行EFS的分层分析
此外,在CAR-T回输后第3天每μL血液中CAR-T细胞的数量与产品初始T细胞百分比增加显著相关(p=0.0488,图7)。
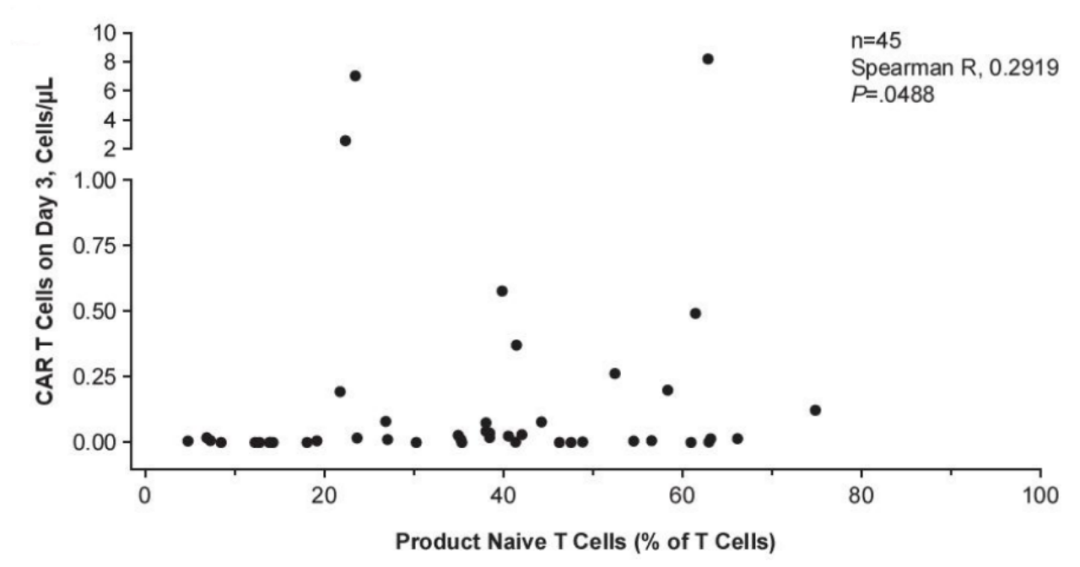
图7 产品初始T细胞百分比与Axi-cel回输后Day 3血液样本中CAR-T细胞数量之间的相关性
Axi-cel血清药效学特征与临床结局的相关性
29种血清炎症与免疫调节生物标志物的分析结果显示,大多数生物标志物水平在Ax-cel回输后迅速短暂升高,在7天内达到峰值水平,并在输注后第4周恢复至基线水平(图8)。需要注意的是,白细胞介素-15(IL-15)与单核细胞趋化蛋白-1(MCP-1)水平可在CAR-T细胞回输前清淋预处理后升高。
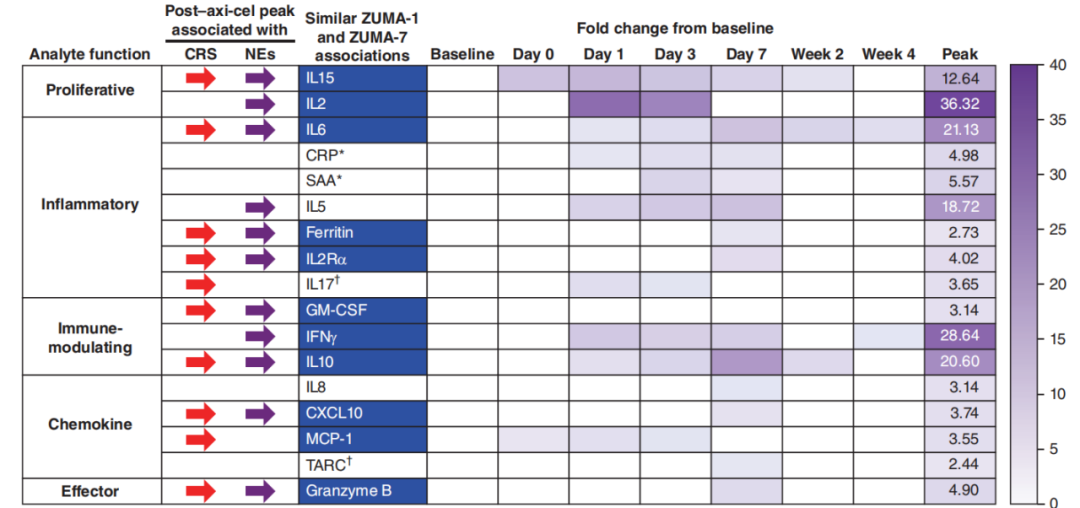
图8 血清生物标志物与≥3级CRS和NEs之间的相关性分析
多种血清生物标志物[如IL-15、IL-6、铁蛋白、粒细胞-巨噬细胞集落刺激因子(GM-CSF)、趋化因子CXC配体10(CXCL10)与干扰素γ(IFNγ)]的峰值(和/或AUC0-28水平),均与≥3级CRS或NEs相关。在部分患者中,血清生物标志物[如细胞间黏附分子-1(ICAM-1)与血管细胞黏附分子-1(VCAM-1)]的峰值水平较基线升高≥2倍,与≥3级不良事件的发生相关。在基线与第0天,肿瘤坏死因子α(TNFα)与INTL2R/CD25水平升高也与较高级别的CRS与NEs发生相关。
与此同时,与疗效存在相关性的血清生物标志物较少,IL-10、IL-5与IL-15水平与疗效(如ORR、完全缓解、持续缓解、EFS和PFS)呈正相关,而IL-7、IL-12p40与巨噬细胞炎性蛋白1B(MIP-1B)与疗效呈负相关。在基线(可选桥接之前的时间点,仅限于糖皮质激素)与第0天(清淋预处理后Axi-cel回输前的时间点),TNFα、MIP-1A、颗粒酶B、MIP-1B、INTL2R/CD25与IL-7水平的升高与疗效降低相关。
此外,在基线及回输后的时间点,较高水平的血清炎症生物标志物与分化程度较高的T细胞,如TCM表型(CCR7+ CD45RA– T细胞)或TEM+TEFF表型(CCR7–T细胞)百分比相关,而初始T细胞表型与许多毒性相关的血清生物标志物呈负相关。
单采血T细胞属性与Axi-cel产品中免疫T细胞亚群之间的相关性
单采中的T细胞表型与Axi-cel产品中的免疫T细胞亚群密切相关(图9a-d)。富含 CD27+ CD28+ CD8+初始T细胞与客观缓解(p=0.0369)与PFS(p=0.0345)相关,但与CRS(p=0.9619)或NEs(p=0.1319)无关。与ZUMA-1研究相比(n=100),ZUMA-7研究中(n=137)单采血细胞中CD27+ CD28+初始T细胞亚群百分比更高,表明在早线治疗中更有可能获得更具干细胞样表型的T细胞产物。

图9 单采血T细胞属性与Axi-cel产品属性之间的相关性(A-D)
研究结论
在LBCL二线治疗中,Axi-cel的疗效与安全性与其产品属性相关。CAR-T细胞扩增峰值与临床缓解和不良事件之间具有相关性。Axi-cel的血清药效学特征与其疗效和不良事件相关。单采血和最终CAR-T产品中表达CD27和CD28的初始T细胞表型(CCR7+ CD45RA+)与更好的疗效、更低的毒性和更早线治疗相关。上述结果支持CAR-T细胞疗法在LBCL患者中早线更获益的观点。
免责声明:本资料为专业医学资料,旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参考;任何处方请参考产品最新详细处方资料。本文件可能包含涉及医学情况、健康及治疗方法的信息。相关信息不得用作诊断或治疗,不能替代专业医学意见。
审批编号:NP-NHL-Axi-Cel-2024.3-8 valid until 2026.3
供稿与审核:临床开发与医学部
推荐阅读
-
肿瘤微环境分析阐释二线Axi-cel与SOC治疗LBCL的疗效差异
-
【2023 ASH】EBMT/Gocart真实世界数据:CD19 CAR-T细胞可有效治疗PCNSL和SCNSL患者
-
【2023 ASH】CIBMTR真实世界证据:LBCL患者在CR状态下接受CAR-T巩固治疗仍可获益
-
【2023 ASH】真实世界证据:CAR-T治疗R/R LBCL获益不受高龄影响
-
【2023 ASH】CAR-T治疗显著改善双打击/三打击淋巴瘤患者生存:早用更获益
-
【2023 ASH】CIBMTR真实世界证据:桥接治疗对Axi-cel治疗R/R LBCL的影响
-
单细胞RNA分析表明第三代CAR-T细胞的内在功能特征与淋巴瘤疗效相关
-
【2023 ASH】ZUMA-1研究6年随访生存数据:Axi-cel点亮难治性LBCL治愈之光
-
【2023 ASH】Axi-cel治疗LBCL:二线 vs 三线,早用更获益
-
【2023 ASH】CAR-T二线治疗R/R LBCL的真实世界证据
-
【2023 ASH】ZUMA-12的3年随访分析展示Axi-cel在一线高危LBCL患者治疗中的风采
-
【2023 ASH】真实世界中Axi-cel治疗LBCL患者的5年随访结局彰显治愈希望
-
【2023 ASH】Brexu-cel治疗R/R B-ALL成人患者的真实世界证据
-
【2023 ASH】CAR-T之声:一文速览Brexul-cel相关研究的最新进展
-
【ASH 2023】CAR-T细胞治疗重塑DLBCL患者的生存趋势
-
【2023 ASH】CAR-T之声:一文速览Axi-cel相关研究的最新进展
-
CAR-T细胞治疗合并肾功能减退的LBCL患者的真实世界结局
-
临床前研究提示来那度胺可改善第三代CD19 CAR-T细胞对DLBCL的疗效
-
【2023 ESMO】治疗3L+ R/R LBCL,Axi-cel vs Glofit,孰优孰劣?
-
Yescarta®全球上市6周年,为淋巴瘤患者点亮治愈的希望之光
-
奕凯达治疗R/R NHL继中国真实世界研究中期分析数据后再添亚裔人群证据,赵维莅等教授评论文章NEJM新发布!
-
CAR-T细胞治疗R/R LBCL的不良预后因素:欧洲 vs 美国患者
-
CAR-T治疗B-NHL的安全性和有效性不受合并自身免疫性风湿性疾病的影响
-
ctDNA可提高Axi-cel治疗R/R LBCL后PET的特异性
-
有效的桥接疗法可改善CAR-T治疗R/R LBCL患者的临床结局

