【2024 EHA】免疫组化检测的CD19阴性对接受Axi-cel治疗的淋巴瘤患者的结局影响
2024年欧洲血液学协会(EHA)年会于当地时间6月13日至16日在西班牙马德里召开,作为全球首屈一指的血液学领域的科学交流盛会,每年都吸引着来自世界各地的专家学者,共同推着血液学科的发展与进步[1]。
大B细胞淋巴瘤(LBCL)是一种高度异质性的血液系统恶性肿瘤,包括弥漫性大B细胞淋巴瘤(DLBCL)、原发性纵隔大B细胞淋巴瘤(PMBCL)和转化后的滤泡性淋巴瘤(tFL)[2]。大约40%左右的LBCL患者在一线治疗后出现复发或耐药,进展为复发/难治性(R/R)LBCL[3]。Axicabtagene ciloleucel(Axi-cel)是一种抗CD19嵌合抗原受体T(CAR-T)细胞疗法,在常规治疗失败后对R/R LBCL有很高的应答率。Axi-cel的CAR结构由单链可变片段细胞外结构域与CD3ζ(也称为CD247)和CD28胞内结构域组成,通过靶向CD19蛋白激活T细胞信号[4]。
小编节选了一篇“壁报”(P1196),让我们一睹真实世界中,通过免疫组化评估CD19表达对Axi-cel治疗R/R LBCL的预后(缓解、毒性和生存)影响。
摘要编号:P1196[5]
英文标题:Impact of CD19 expression by immunohistochemistry in lymphoma patients treated with axicabtagene ciloleucel
中文标题:免疫组化方法检测的CD19表达对接受Axicabtagene ciloleucel治疗的淋巴瘤患者的结局影响
研究背景
以CD19为靶点的自体CAR-T细胞疗法改善了R/R LBCL的预后。在既往临床研究中,通过免疫组织化学法(IHC)测定的CD19抗原表达缺失并不是CAR-T细胞疗法的排除标准。然而,尚未有研究直接比较CD19表达与否对CAR-T治疗R/R LBCL的结局影响。
研究方法
研究纳入了2019年12月至2023年9月期间在Clínico瓦伦西亚大学医院接受商业化Axi-cel治疗且至少进行过一次CD19-IHC活检的R/R LBCL成年患者。CD19克隆LE-CD19用于CD19-IHC染色,对于存在多次活检结果的患者,优先考虑采用最接近CAR-T细胞回输时的活检结果。桥接治疗后未行活检。所有样本均由两名独立的病理学专家进行集中分析,并生成一份报告,其中包括对阳性百分比的半定量评估结果。前瞻性地收集有关患者和疾病特征、治疗过程和临床结果的数据。
根据CD19-IHQ表达情况(阴性与任意程度阳性)对患者进行分组后再行统计学比较分析。其中,连续变量组间比较采用Mann-Whitney分析,分类变量组间比较采用Fisher精确检验和卡方检验。
研究结果
研究共纳入47例成人R/R LBCL患者(弥漫大B细胞淋巴瘤,n=40;原发性纵隔大B细胞淋巴瘤,n=7)。
患者基线特征见表1。患者中位年龄为62岁(范围,22岁-77岁),25例(53%)为原发难治性患者,13例(28%)患者为Myc基因重排,45例(96%)患者接受了桥接治疗。最后一次CD19-IHC活检至CAR-T回输之间的中位治疗线数为0线(范围,0线-3线)。
表1 患者基线特征
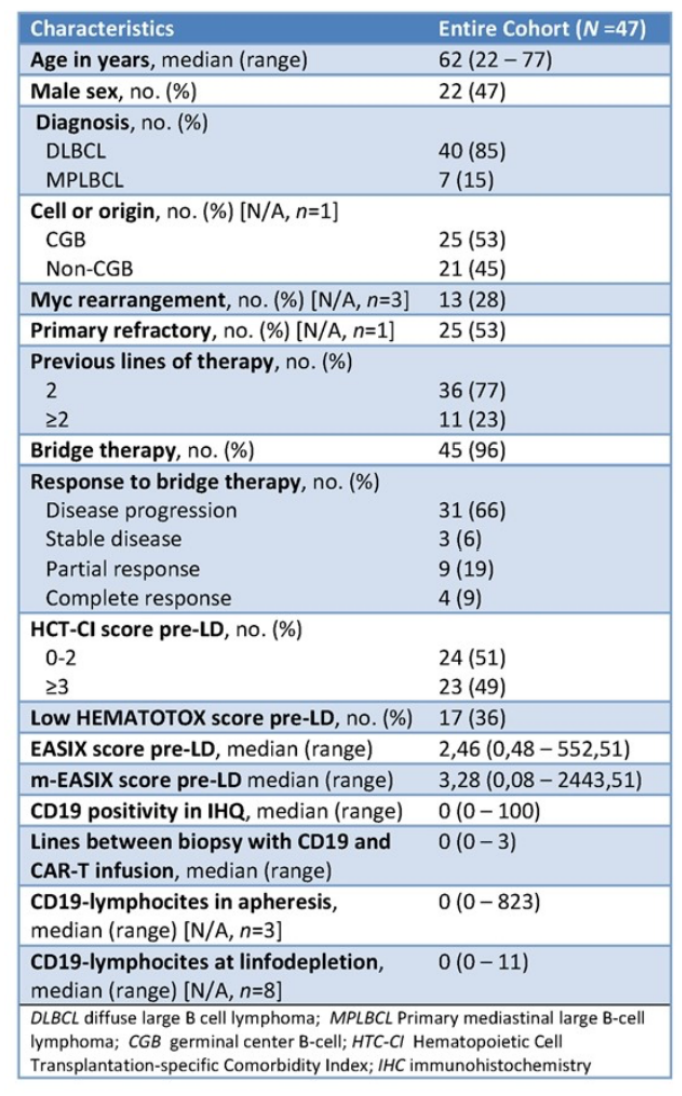
IPI≤1的患者(p=0.037)和CAR-T回输前接受过≥1线治疗的患者的活检中,CD19-IHC表达显著升高(p=0.016)。
患者的中位随访时间为206天(范围,58天-1157天)。CD19-IHC阳性组和阴性组在细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性综合征(ICANS)、客观缓解率(ORR)、总生存期(OS)或无进展生存期(PFS)等结局上没有统计学差异(表2)。
表2 全队列和CD19表达亚组队列中ORR、CRS和ICANS的发生率比较
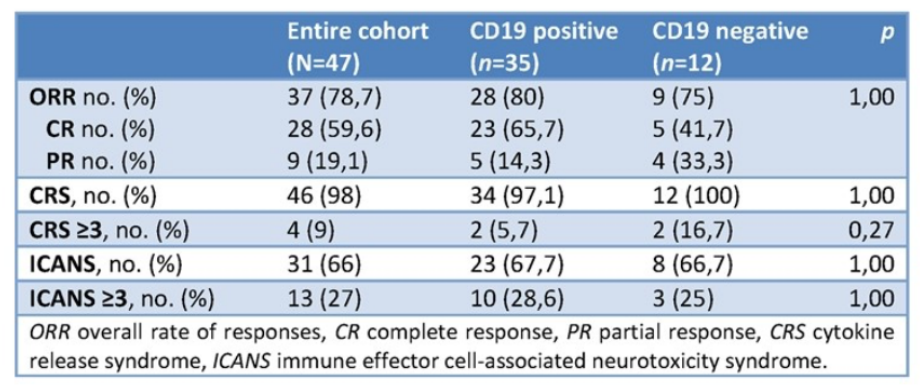
注:ORR,客观缓解率;CRS,细胞因子释放综合征;ICANS,免疫效应细胞相关神经毒性综合征
研究结论
本研究表明经免疫组化检测的CD19表达缺失(阴性)的患者接受Axi-cel治疗后依然具有良好的疗效和安全性,且与CD19表达阳性患者无统计学差异。因此,CD19免疫组化表达阴性不应成为临床医生拒绝为LBCL患者提供CD19 CAR-T细胞治疗的理由。
讨 论
CD19在正常B细胞、肿瘤B细胞以及滤泡树突状细胞中特异性表达,是B细胞最可靠的表面生物标记物之一,所以靶向CD19的CAR-T细胞治疗可有效的治疗B细胞肿瘤。肿瘤的 CD19 表达水平具有异质性,流式细胞术检测显示一部分肿瘤的表达水平较低。敏感性较差的检测技术,例如免疫组织化学染色 (IHC),可能无法检测到这些低水平的抗原表达。
在ZUMA-1研究中,共101例患者接受CAR-T细胞回输,其中DLBCL 77例,PMBCL或tFL 24例[4]。82例患者进行了CD19免疫组化表达分析,其中8例(10%)为CD19阴性,74例(90%)为CD19阳性。亚组分析表明,74例CD19阳性的患者在CAR-T回输后,ORR为0.85(95% CI,0.75-0.92);8例CD19阴性患者在CAR-T回输后,ORR为0.75(95% CI,0.35-0.97)(图1)。在8例CD19阴性患者中观察到的应答率与CD19阳性疾病患者相似,这表明免疫组化方法检测CD19表达的潜在局限性,免疫组化方法检测出来的CD19阴性不是真正的CD19阴性[4]。由于IHC显示CD19抗原表达水平低至不可检测的患者可能对 Axi-cel有反应,因此ZUMA-1研究方案未排除此类患者。如果既往进行过CD19靶向治疗,可以考虑通过灵敏度更高的技术检测CD19。

图1 ZUMA-1研究中关键基线和临床协变量的客观缓解率的亚组分析
免责声明:本资料为专业医学资料,旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参考;任何处方请参考产品最新详细处方资料。本文件可能包含涉及医学情况、健康及治疗方法的信息。相关信息不得用作诊断或治疗,不能替代专业医学意见。
审批编号:NP-NHL-Axi-Cel-2024.7-12 valid until 2026.7
供稿与审核:临床开发与医学部
推荐阅读

