打破困局:CAR-T细胞疗法赋能不适合ASCT的淋巴瘤治疗
自体造血干细胞移植(ASCT)是一线免疫化疗后复发/难治性弥漫性大B细胞淋巴瘤(R/R DLBCL)患者的标准治疗方案[1]。目前,只有约10%的R/R DLBCL患者接受ASCT治疗后达到治愈[2]。因此,亟需新的治疗方案以提高治疗效果。
嵌合抗原受体T(CAR-T)细胞疗法是一种新型的免疫治疗手段。近年来,CAR-T细胞疗法在不适合接受ASCT患者中的应用得到了广泛研究,使更多患者临床获益,成为一种有效的治疗选择[1]。因此,本文旨在识别不适合ASCT但适合接受CAR-T细胞疗法的患者群体,并探索CAR-T细胞疗法在这一患者群体中的疗效。
表1 不适合ASCT但适合CAR-T细胞疗法的患者[1]
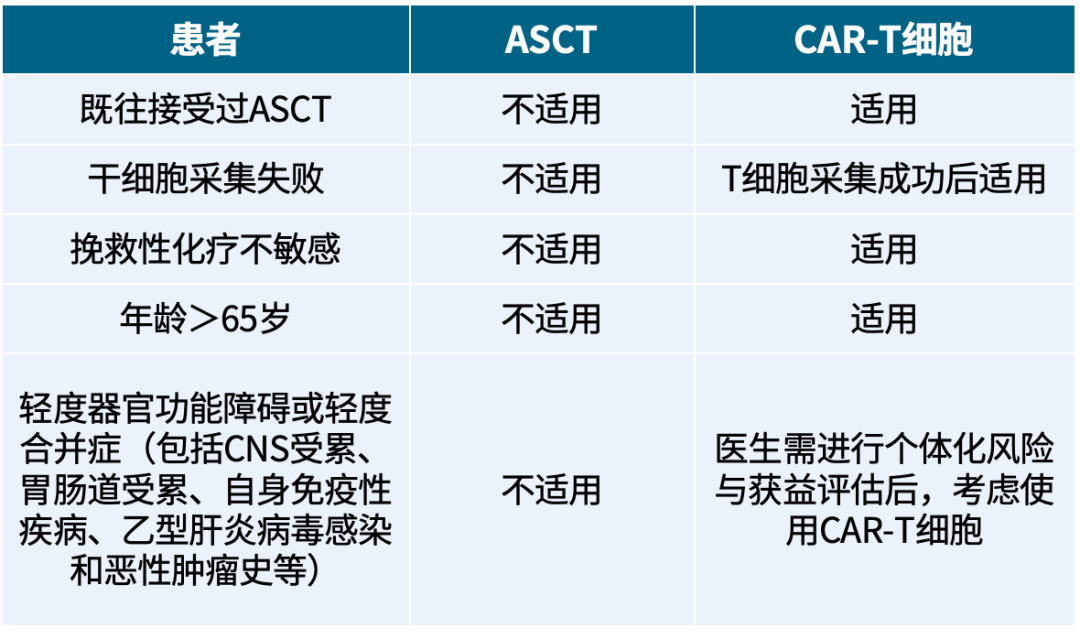
ASCT:自体造血干细胞移植;CAR-T细胞:嵌合抗原受体T细胞;CNS:中枢神经系统。
既往接受过ASCT的患者通常被认为不适合再次接受ASCT,但可选择CAR-T细胞疗法[1]。一项前瞻性研究共纳入49例R/R B细胞淋巴瘤患者,在第0天回输自体干细胞,并于第1天回输CAR-T细胞。治疗后3个月时,客观缓解率(ORR)为81.6%,完全缓解(CR)率为77.6%,3年总生存期(OS)率和无进展生存期(PFS)率分别为72.3%和66.6%,≥3级细胞因子释放综合征(CRS)和≥3级免疫效应细胞相关神经毒性综合征(ICANS)发生率分别为22.4%和4.1%。结果提示CAR-T细胞治疗前可以接受ASCT,且具有良好疗效和安全性[3]。
对于挽救性化疗不敏感的患者无法获益于ASCT,但可能从CAR-T细胞疗法中获益[1]。一项真实世界研究共纳入1001例大B细胞淋巴瘤(LBCL)患者,其中66%患者伴有化疗耐药。中位随访12个月时,对于化疗耐药患者,ORR为66%、CR率为48%,12个月PFS率和OS率分别为40%和54%,提示CAR-T细胞疗法治疗化疗耐药患者的总体预后均良好[4]。
年龄>65岁是限制接受ASCT的标准,但并不影响患者接受CAR-T细胞治疗[1]。一项前瞻性研究共纳入493例接受CAR-T细胞治疗的R/R LBCL患者,中位随访24.5个月时,年龄≥65岁的患者与年龄<65岁的患者相比,ORR(82% vs 75%)和CR率(68% vs 56%)在数值上更高,提示CAR-T细胞可作为高龄R/R LBCL患者的有效治疗方案[5]。
轻度器官功能障碍或轻度合并症的患者可能不适合进行ASCT,但可以考虑采用CAR-T细胞疗法[1]。例如,一项荟萃分析共纳入141例接受CAR-T细胞治疗的中枢神经系统(CNS)受累的LBCL患者,结果显示,ORR和CR率分别为61%和55%,中位OS和中位PFS分别为8.8个月和4.4个月,10%患者发生≥3级CRS,25%患者发生≥3级ICANS,提示对于CNS受累的LBCL患者,CAR-T细胞疗法具有良好的疗效和安全性,且与其他研究中非CNS受累患者的结果相似[6]。
结 论
对于R/R DLBCL患者,ASCT与CAR-T细胞疗法提供了两种治疗选项。鉴于部分患者因多种因素不适合接受ASCT,CAR-T细胞疗法成为其重要的治疗选择。多项临床研究已证实,在不适合ASCT的患者群体中,CAR-T细胞疗法展现了良好的疗效和安全性。因此,精准识别那些不适合ASCT但适合CAR-T细胞疗法的患者,对于为其提供个性化治疗方案、优化医疗资源配置、缩短治疗周期、提升患者生活质量及延长生存期具有重要意义。
免责声明:本资料为专业医学资料,旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参考;任何处方请参考产品最新详细处方资料。本文件可能包含涉及医学情况、健康及治疗方法的信息。相关信息不得用作诊断或治疗,不能替代专业医学意见。
审批编号:NP-NHL-Axi-Cel-2024.12-4 valid until 2026.12
供稿与审核:临床开发与医学部

