CAR-T细胞治疗LBCL增效策略之联合BTKi±PD-1i的探索
近年来,嵌合抗原受体T(CAR-T)细胞疗法在复发/难治性大B细胞淋巴瘤(R/R LBCL)治疗中展现出显著的疗效,但部分患者疗效不佳与肿瘤微环境(TME)密切相关。TME中的免疫抑制因素,如高表达抑制性受体的耗竭T细胞和M2型巨噬细胞等,会限制CAR-T细胞的活性和疗效。布鲁顿酪氨酸激酶抑制剂(BTKi)通过调节TME中免疫细胞的组成和功能,有望与CAR-T细胞治疗产生协同作用。而程序性细胞死亡受体1抑制剂(PD-1i),与CAR-T细胞治疗联合可增加外周血CAR-T细胞计数,提升疗效。因此,联合BTKi±PD-1i以增强CAR-T细胞治疗效果的探索显得尤为重要。《Clin Transl Med》近期发表了一项临床研究,该研究采用基于CAR-T治疗后应答调整的泽布替尼±替雷利珠单抗联合方案治疗R/R LBCL,其疗效和安全性如何?让我们一探究竟[1]。
研究设计
该研究为一项回顾性、单中心观察性研究,共纳入54例CD19阳性R/R LBCL成人患者(图1)。所有患者在接受CAR-T细胞治疗后,采用基于应答调整的治疗方案(ZRTI组):自单采至CAR-T细胞回输后第28天,每日口服泽布替尼320 mg;在第28天疗效评估时,36例(66.7%)达到完全缓解(CR)的患者继续接受泽布替尼单药维持治疗3个月,15例(27.8%)达到部分缓解(PR)的患者则在泽布替尼治疗基础上联合雷利珠单抗(200mg,每3周1次,最长持续2年)治疗;3 例(5.6%)疾病稳定(SD)或疾病进展 (PD) 的患者接受后续抗肿瘤治疗。研究评估了患者的客观缓解率(ORR)、完全缓解(CR)率、无进展生存期(PFS)、总生存期(OS)及安全性,并对 43 例患者的肿瘤样本进行DNA测序,对25例患者样本进行RNA测序,分析基因异常和TME特征。
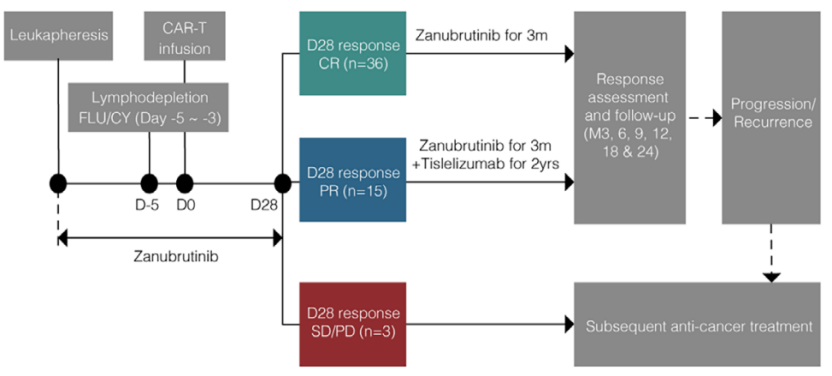
图1 基于CAR-T治疗后应答的适应性联合BTKi±PD-1i研究设计示意图
疗 效
在ZRTI组中,第28天、第3个月和第6个月的ORR分别为94%(CR:66%,PR:28%)、87%(CR:80%,PR:7%)和 80%(CR:76%,PR:4%)(图2)。在15例第28天评估为PR的患者中,10例(66.7%)患者在加用替雷利珠单抗后转为CR。中位随访23.6个月时,估计的2年PFS率和OS率分别为68%和76%,中位PFS和中位OS均未达到。
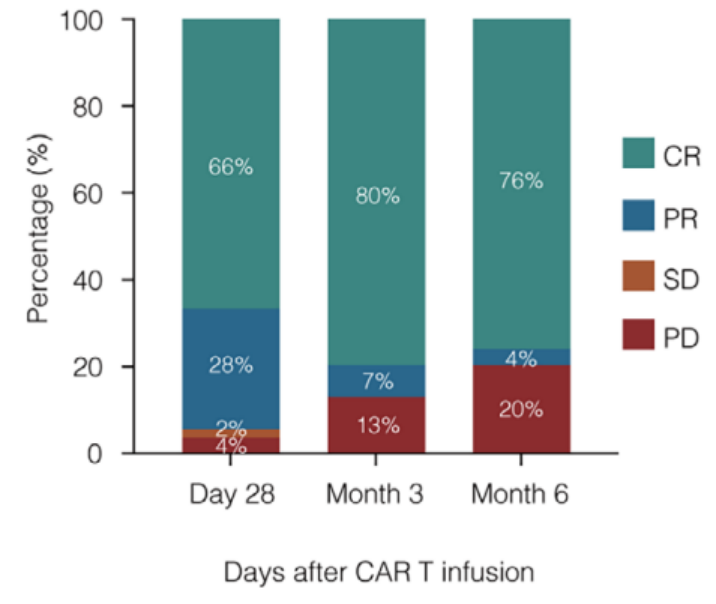
图2 治疗缓解率
安全性
在ZRTI组中,治疗期间未发现新的安全性信号。任何等级细胞因子释放综合征(CRS)发生率为85%(其中≥3级CRS为9%),任何等级免疫效应细胞相关神经毒性综合征(ICANS)发生率为13%(未发生≥3级ICANS)。在36例接受泽布替尼单药治疗的患者中,未发生治疗中断。在15例接受联合治疗的患者中,5例发生治疗中断。联合治疗未增加不良事件。
单因素和多因素分析治疗结局的预测因素
在ZRTI组中,单因素和多因素分析均显示,大包块(Dmax > 4.0 cm)与较差的PFS(p=0.0005和p=0.0045)和OS(p=0.0141和p=0.0451)显著相关。进一步分析发现,与非大包块患者相比,大包块患者的耗竭T细胞(p=0.0329)和M2型巨噬细胞(p=0.0149)标志物表达显著升高,提示大包块患者TME的免疫抑制性更强。
在ZRTI组可评估的43例患者中,21例(49%)患者为TP53突变型,6例(14%)为MCD型,4例(9%)为BN2型,1例(2%)为N1型,3例(7%)为EZB型,2例(5%)为ST2型,6例(14%)为NOS型。不同基因型的CR率、ORR、PFS和OS均无显著差异。
泽布替尼±替雷利珠单抗对TME的影响
对25例ZATI 组患者肿瘤样本进行了RNA测序。结果显示,泽布替尼单药与联合治疗患者的TME中耗竭T细胞、调节性T细胞(Treg)、M2型巨噬细胞和髓系来源抑制细胞(MDSC)均无显著性差异。
研究同时纳入了22例未使用泽布替尼或替雷利珠单抗治疗的但接受CAR-T细胞治疗的CD19阳性R/R LBCL患者作为对照(非ZATI组)。研究表明,在非ZATI组中,与应答者(CR和PR)相比,无应答者(SD和PD)耗竭T细胞标志物表达显著升高(p=0.0230),且高表达者PFS较差(p=0.0074);而ZATI组无此相关性。再者,与应答者相比,两组无应答者M2巨噬细胞标志物表达均显著增加(非ZATI组:p=0.0103,ZATI组:p=0.0203),且高表达者PFS较差(非ZATI组:p=0.0004,ZATI组:p=0.0157)。两组Treg和MDSC均与疗效无相关性。结果表明,基于应答调整的泽布替尼±替雷利珠单抗方案可有效减少耗竭T细胞,但无法克服M2型巨噬细胞介导的免疫抑制作用。
泽布替尼±替雷利珠单抗对耗竭T细胞亚群的影响
在非ZATI组中,与应答者相比,无应答者的抑制性受体PDCD1(p=0.0082)和LAG3(p=0.0279)表达显著升高,中间耗竭T细胞(p=0.0075)和终末耗竭T细胞(p=0.0045)比例也显著增加,且伴随T细胞功能、细胞因子信号通路等抗肿瘤免疫应答的广泛失调。而在ZATI组中,抑制性受体和耗竭T细胞亚群均与应答者无相关性。提示泽布替尼±替雷利珠单抗有效减少抑制性受体和耗竭T细胞亚群。
脂质代谢改变对M2型巨噬细胞的影响
在ZATI组中,与应答者相比,无应答者TREM2表达显著升高(p=0.0294),而与MARCO、STAB1和SELPLG无相关性。对CAR-T细胞回输前肿瘤活检标本进行免疫组织化学分析显示,与应答者相比,无应答者的TREM2+(p=0.0350)和M2型巨噬细胞标志物CD163+(p=0.0092)表达水平升高,且二者呈正相关,表明TME内富集了TREM2+ M2型巨噬细胞。此外,TREM2表达升高与脂质代谢相关基因水平高(APOC1、APOE和GPNMB)显著相关。这些结果表明,TREM2+ M2巨噬细胞通过脂代谢重编程塑造免疫抑制性微环境,可能是导致CAR-T细胞治疗耐药的关键因素。
小 结
研究表明,基于应答适应性调整的泽布替尼±替雷利珠单抗方案可增强CAR-T细胞疗法对R/R LBCL患者的疗效,且安全性良好。该联合方案主要是通过减少TME中的耗竭T细胞实现的。研究同时揭示TREM2+ M2巨噬细胞通过脂质代谢重编程介导耐药,为通过调控免疫代谢以优化CAR-T细胞疗法提供了重要理论依据。
免责声明:本资料为专业医学资料,旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参考;任何处方请参考产品最新详细处方资料。本文件可能包含涉及医学情况、健康及治疗方法的信息。相关信息不得用作诊断或治疗,不能替代专业医学意见。
审批编号:NP-NHL-Axi-Cel-2025.5-16 valid until 2027.5
供稿与审核:临床开发与医学部

